- 2012年度
- 大脳皮質の進化の謎に迫る
(2013/03/29) - 活性型ビタミンDで小胞体ストレスを緩和しよう!
(2013/03/29) - Sweat Glands Grown from Newly Identified Stem Cells
(2013/03/29) - ~筋肉の恒常性と健康は相反するものなのか?~ 筋肉においてオートファジーが存在するが故にインスリン抵抗性が存在する
(2013/03/29) - たった1つの因子の抑制で様々な細胞が神経に!?
(2013/03/28) - 乳酸菌を取り込むと、細胞も若返る?! ~"人間、またしても発酵食品のお世話になる"の巻~
(2013/03/27) - 脳腫瘍における新しい遺伝子変異~エピジェネティク
(2013/03/27) - CCR2-dependentrecruitment of macrophages by tumor-educated mesenchymal stromal cells promotes tumor development and is mimicked by TNFα
(2013/03/25) - 補体C1qはWntシグナルの活性化を介して細胞を老化させる
(2013/03/19) - Speramtogonial Stem Cell Transplantation into Rhesus Testes Regenerates Spermatogenesis Producing Functional Sperm.
(2013/03/12) - 糖尿病薬剤による抗腫瘍効果
(2013/03/12) - 難病ALSの新たな原因遺伝子の発見
(2013/03/12) - 脊髄損傷にヒートショックプロテインが有効?
(2013/03/11) - 片頭痛患者では血管内皮前駆細胞が少ない?
(2013/03/11) - 筋幹細胞の静止状態はmiRNA-489により維持される
(2013/03/11) - ストレスに弱いってどういうこと?(心の病気にかかるメカニズムの一つ、「ストレス脆弱モデル」をネズミで再現)
(2013/03/09) - 核酸医薬は実現するか~筋強直性ジストロフィー治療の可能性~
(2013/03/09) - なくならないのは技がある!
(2013/03/08) - Down症候群のiPS細胞の染色体数を修正する
(2013/03/08) - 高品質なiPS細胞作製のキーファクターZscan4の同定
(2013/03/08) - Turning off the Neuron Death Pathway
(2013/03/07) - 新しい安全な分子標識-マルチ同位体画像質量分析法-が明らかにした幹細胞の不等分裂様式
(2013/03/07) - 重度脊髄損傷後に移植した神経幹細胞が非常に長く軸索を伸長し、シナプス結合した!
(2013/03/07) - 神経系前駆細胞を元気にして水頭症を治す!?
(2013/03/05) - FUS/TLSとTDP-43 二つのALS原因遺伝子の交差点
(2013/03/01) - 貪食細胞マクロファージが造血幹細胞を優しく包み込んで自己複製能の維持に貢献していた!?
(2013/02/27) - TALENs -新遺伝子改変技術が生命科学を変える!?-
(2013/02/27) - RESTタンパク質による遺伝子発現調節 ~遺伝子発現とシナプス機能~
(2013/02/25) - 腸に住んでいるある平凡な細菌によって大腸がんは引き起こされる!
(2013/02/25) - 癌抑制遺伝子p53の変異はメバロン酸経路を活性化することで、正常な乳腺の構造を失わせる
(2013/02/25) - 樹状細胞は制御性T細胞の恒常性をコントロールすることで多発性硬化症を寛解させる
(2013/02/25) - Schwann Cell Plasticity After Spinal Cord Injury Shown by Neural Crest Lineage Tracing
(2013/02/15) - エクソソームは、癌細胞の「飛び道具」!
(2013/02/08) - 老化したニッチでは筋肉幹細胞は静止状態を保てない
(2013/01/31) - 幹細胞を使った創薬開発
(2013/01/31) - 体細胞リプログラミングにおける遺伝子発現調節の解析からわかること-single cellで見てみようの巻-
(2013/01/31) - がん幹細胞発生のかぎを握るのは誰?-ユーイング肉腫がん幹細胞の解析を通じた検証-
(2013/01/31) - 小動物用PET(Positron Emission Tomography)で、ラットの脳梗塞巣を探知することができる [18F]BMS-PET
(2013/01/31) - 脳の神経ネットワークにおけるヤングパワー!
(2013/01/18) - アストロサイトの性格はどうやって決まる?
(2013/01/18) - 幹細胞の自己複製能を制御する因子とは?
(2013/01/18) - アルデヒドが真犯人!?DNA損傷と再生不良性貧血
(2012/12/18) - HIV-2の新しい定量法
(2012/12/18) - Japanese People's Preference for Place of End-of-Life Care and Death: A Population-Based Nationwide Survey
(2012/12/18) - がん細胞の死に際
(2012/12/18) - 癌幹細胞を眠りから目覚めさせる"Coco"
(2012/12/13) - 細胞接着分子のインテグリンが血液の幹細胞の維持を制御する
(2012/12/11) - 移植された神経幹細胞は免疫系にも作用する
(2012/12/11) - 血液がん克服にむけて!~JAK2阻害剤の薬剤耐性メカニズム解明~
(2012/12/04) - 癌進展を陰で操る支配者
(2012/11/30) - 幹細胞の2つの顔を暴け!!! 未分化性維持と特異的分化との狭間で...
(2012/11/30) - 脊髄損傷後の機能回復には自発的なリハビリが効果的
(2012/11/21) - もしあなたの歯が無くなってしまった時に...
(2012/11/15) - iPS細胞から血小板をつくる
(2012/10/30) - メラノーマのエキソソームで予後予測ができる?!
(2012/10/30) - Oligodendroglia Cells Can Do Much More Than an Insulator for Neuron
(2012/09/11) - APJは、心臓肥大のデュアル受容体として作用する
(2012/09/11) - 幹細胞医療;脳梗塞治療への挑戦
(2012/09/11) - 造血幹細胞の老化と若返り
(2012/09/11) - カロリー制限が筋肉を増やす? - トレーニング界の常識に挑戦する新たな"逆説"
(2012/09/11) - 癌幹細胞は治療標的にならない!?
(2012/08/24) - iPS細胞でC型肝炎ウイルス感染のモデルをつくる
(2012/08/09) - ES細胞、iPS細胞から内耳有毛細胞への分化誘導
(2012/08/09) - 造血幹細胞を冬眠させる細胞はなんと神経系の細胞だった!
(2012/07/06) - 個別化治療への障壁 ~多重人格なガンを克服せよ~
(2012/07/06) - 栄養のバランスが新しいニューロンを作り、体重や新陳代謝をコントロールする
(2012/05/11) - 脊髄不全損傷後におこる、残存神経ネットワークの代償機能
(2012/05/11) - "スーパーPTENマウス"
(2012/04/20) - 統合失調症iPS細胞研究が臨床研究になるために
(2012/04/20) - 発癌機序における"はじめの一歩"
(2012/04/06) - iPS細胞は脊髄損傷を治せるのか?
(2012/04/06)
- 大脳皮質の進化の謎に迫る
- 2011年度
- 2010年度
ホーム > 世界の幹細胞(関連)論文紹介 > 幹細胞の2つの顔を暴け!!! 未分化性維持と特異的分化との狭間で...
幹細胞の2つの顔を暴け!!! 未分化性維持と特異的分化との狭間で...
論文紹介著者

吉田 剛(博士課程 2年)
GCOE RA
先端医科学研究所 遺伝子制御部門
第一著者名・掲載雑誌・号・掲載年月
Kohei Yamamizu/Cell Stem Cell, 10: 759-770, 2012
文献の英文表記:著者名・論文の表題・雑誌名・巻・号・ページ・発行年(西暦)
Protein kinase a determines timing of early differentiation through epigenetic regulation with G9a.
Kohei Yamamizu, Mayako Fujihara, Makoto Tachibana, Shiori Katayama, Akiko Takahashi, Eiji Hara, Hiroshi Imai, Yoichi Shinkai, Jun K. Yamashita
Cell Stem Cell, 10:759-770, 2012
論文解説
個体発生初期の胚盤胞(blastocyst;※1)の内細胞塊(inner cell mass; ICM)に由来する、自己複製能と多分化能を備えたES細胞(embryonic stem cell;※1参照)は、個体の発生を研究する上で非常に有用であり、臨床的にも再生医療への応用性が期待されて久しい。しかしながら、サイトカイン(※2)の刺激などによって特定の細胞に分化(lineage-committed differentiation)を遂げる際に、エピジェネティックレベルでの協調的かつ精密な制御が行われていると考えられている。
1940年代にイギリスEdinburgh大学のConrad Waddington博士は、世界で初めて"エピジェネティックス(※3)"を、「表現型を取り込む環境と遺伝子との相互作用」であると定義した。生体を取り囲む環境によって後天的に生み出される生物学的特徴を"獲得形質(acquired phenotype)"と呼ぶが、Waddington博士はこの獲得形質が遺伝すると強烈に主張していた学者の一人であった。彼の哲学的な概念は"Waddington's epigenetic landscape(図1)"として現在の最先端のエピジェネティックス研究者の間でも支持され続けている。
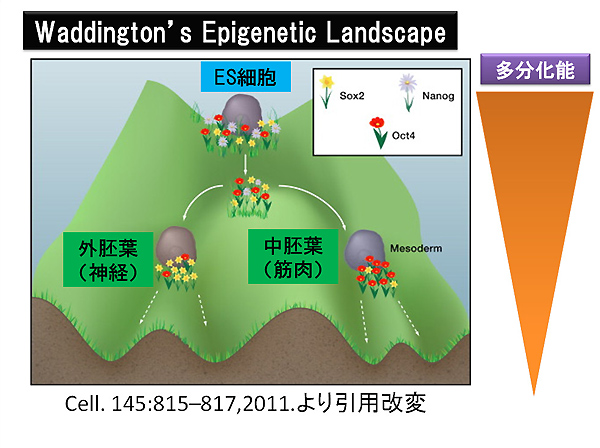
今回紹介する論文では、PKA(protein kinase A)(※4)シグナルの活性化によるエピジェネティック修飾因子G9aの発現増加が、未分化性を維持する上で重要な遺伝子であるOct3/4およびNanogの発現を抑制することで、ES細胞が分化の方向に傾くこと(図2)を証明している。本論文のインパクトは、細胞内シグナル伝達がエピジェネティック修飾因子の発現制御を介して、ES細胞特異的な転写因子の発現をエピジェネティックに抑制していることを明らかにした点であるといえる。
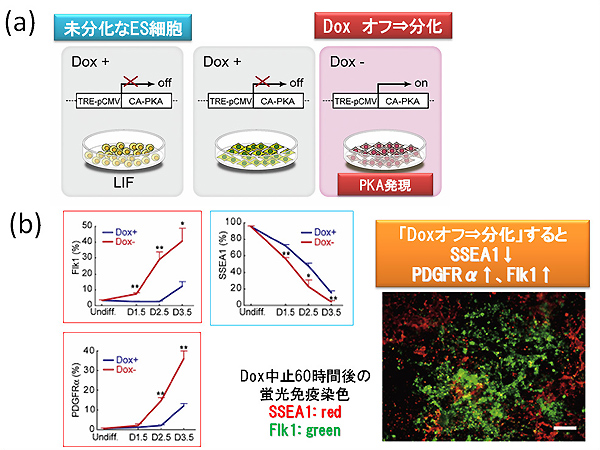
筆者らはまず、TET-OFFシステム(図2-a,※5)を用いて、LIF(leukemia inhibitory factor,※6)の存在下でドキシサイクリン(Dox)投与を中止すると、PKAが発現するような遺伝子改変ES細胞を作製した。Dox投与中止して60時間後に、PKAシグナルを活性化させるcAMPの細胞内濃度が急激に増加し、それに伴って、未分化性マーカーであるSSEA1の発現低下および細胞分化に関与するVEGF受容体Flk1、PDGF受容体の発現増加が認められた(図2-b)。背景にある未分化性維持に重要とされる転写因子Oct3/4とNanogの発現を検討したところ、PKAシグナルの活性化に伴い発現が顕著に低下していた(図3)。興味深いことに、その原因はOct3/4およびNanogのプロモーター領域におけるヒストンH3の9番目のリジンのジメチル化(H3K9me2)であった。すなわち、細胞がWaddington's epigenetic landscapeを「下山」して分化する過程で、活性化PKAシグナルはヒストンメチル化酵素であるG9aの発現を増加させることで、Oct3/4およびNanogの遺伝子プロモーター領域におけるヒストンメチル化を誘導することが明らかとなった。
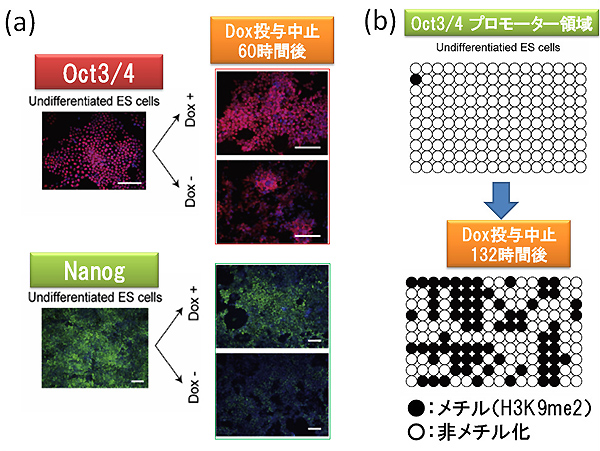
さらに筆者らはES細胞が未分化性を維持しつつ自己複製能を発揮している状態から、特定の細胞系譜に分化して細胞増殖する状態に変化するというphenotype shiftが本当にヒストンメチル化酵素であるG9aを介する活性型PKAシグナルに依存するものであるかどうかを検討するために、タモキシフェン(4-OHT)誘導型のコンディショナルG9aノックアウトES細胞(図4)を作製した。この特殊な遺伝子改変を施したES細胞に対するDoxおよび4‐OHT処理の有無で、未分化維持に必要な転写因子Oct3/4の発現を検討した。その結果、Dox投与中止でPKA発現が陽性である細胞群のうち、4‐OHTを投与しない細胞群ではG9a発現が正常であり、Oct3/4プロモーター領域のヒストンメチル化が亢進していた(図4)。すなわち、Doxおよび4‐OHTを投与しなかった遺伝子改変ES細胞でのみ、Oct3/4発現が抑制された。同様の実験系に基づいてNanog発現を検討したところ、やはりG9aを介するPKAシグナル活性化が分化誘導に重要であることが明らかとなった。
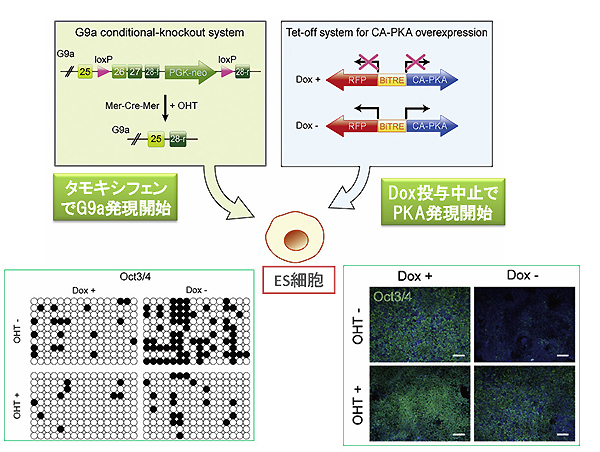
以上の事実から、本論文によって、PKAシグナル伝達はヒストンメチル化酵素であるG9aの発現を促進することで、山中4因子としても知られる未分化マーカーであるOct3/4およびNanogの発現をエピジェネティックに抑制することで、細胞分化のタイミングが制御されていることが明らかになった。Epigenetic Landscapeを降下していく、すなわち分化していくES細胞の分化のタイミングを人為的に制御することが可能であることが強く示唆され、再生医療への応用が大いに期待されるところである。
用語解説
- ※1 胚盤胞:
生物の初期発生過程において卵割が起きてから着床前の胚形成初期に形成される構造であり、ヒトの場合、70-100個の細胞を含有する塊より生じる。栄養膜と内細胞塊からなり、内細胞塊は身体のあらゆる細胞に分化する能力(多分化能)を有することが知られており、ES細胞として樹立され再生医療の分野で注目を浴びている。 - ※2 サイトカイン:
免疫反応や炎症反応に深く関与する免疫システム細胞で産生分泌されるタンパク質である。炎症性サイトカインとしてはIL-1βやIL-6、TNF-αなどが非常に有名である。第17回2012年度慶應医学賞を受賞されたSteven Rosenberg博士の研究領域である「腫瘍免疫療法」の一つとして腎癌に対するIL-2(インターロイキン2)、IFN-α(インターフェロンα)が古くから知られている。 - ※3 エピジェネティックス:
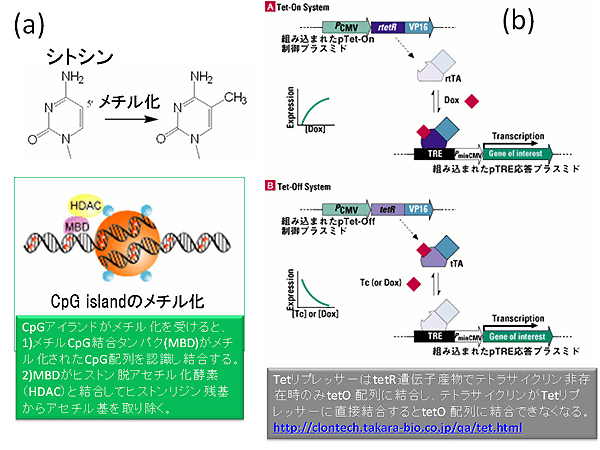
エピジェネティクス(Epigenetics)とは、DNAのプロモーター領域やそれを取り巻くヒストンの化学的修飾によって、DNA塩基配列の違いに依存しない遺伝子発現の多様性を生み出す機構である。最も代表的なものがDNAのメチル化である。真核生物の遺伝子のプロモーター領域に多く見られる5'‐CG‐3'配列は「CpGアイランド」と呼ばれ、このシトシンの5'の位置にメチル基が付加される(図5-a)と、プロモーターは活性を失い、その遺伝子の転写は抑制される。プロモーター領域にCpGアイランド(図5-a)を持つ遺伝子の多くは、組織細胞普遍的に発現しているハウスキーピング遺伝子により偏っていることが知られている。一方で本論文で注目されているヒストンに対するエピジェネティック制御は可逆的であり、Epigenetic Landscapeに従って個体発生段階を経て時間、器官組織依存的に変化する。
- ※4 PKA:
cAMP依存性に活性化されるタンパクキナーゼである。標的タンパク質のセリン/スレオニン残基をリン酸化することで、cAMPを介した細胞内シグナル伝達を司る酵素である。 - ※5 TET-OFFシステム:
ヘルペスウイルス由来のVP16 転写活性化ドメインをTetリプレッサータンパク質と融合させて転写活性化因子(r)tTAとして働かせる。そして培地中の薬剤(テトラサイクリン/ドキシサイクリン)の濃度を調節することによって、TREプロモーター下流に組み込んだ目的の遺伝子の発現レベルを定量的に調節することができるシステムである(図5‐b)。極めて厳しく調節された発現レベルのもとで、「非誘導時の発現(いわゆる"リーク")」は認めない。逆に薬剤誘導すると、速やかに目的遺伝子の発現が調節される。 - ※6 LIF:
マウスのES細胞は、白血病阻害因子(leukemia inhibitory factor, LIF)の存在下では未分化性を保ちながら自己複製するのとは対照的に、LIF非存在下では神経、血球、脂肪細胞などの特定の細胞系譜に従って分化する。LIFを除いた培地でES細胞を浮遊培養すると、ES細胞の集合体である胚様体(Embryoid body;EB)が形成され、胚様体中の細胞が徐々に胚体外内胚葉や原始外胚葉へと分化していく。
Copyright © Keio University. All rights reserved.
