- 2012年度
- 大脳皮質の進化の謎に迫る
(2013/03/29) - 活性型ビタミンDで小胞体ストレスを緩和しよう!
(2013/03/29) - Sweat Glands Grown from Newly Identified Stem Cells
(2013/03/29) - ~筋肉の恒常性と健康は相反するものなのか?~ 筋肉においてオートファジーが存在するが故にインスリン抵抗性が存在する
(2013/03/29) - たった1つの因子の抑制で様々な細胞が神経に!?
(2013/03/28) - 乳酸菌を取り込むと、細胞も若返る?! ~"人間、またしても発酵食品のお世話になる"の巻~
(2013/03/27) - 脳腫瘍における新しい遺伝子変異~エピジェネティク
(2013/03/27) - CCR2-dependentrecruitment of macrophages by tumor-educated mesenchymal stromal cells promotes tumor development and is mimicked by TNFα
(2013/03/25) - 補体C1qはWntシグナルの活性化を介して細胞を老化させる
(2013/03/19) - Speramtogonial Stem Cell Transplantation into Rhesus Testes Regenerates Spermatogenesis Producing Functional Sperm.
(2013/03/12) - 糖尿病薬剤による抗腫瘍効果
(2013/03/12) - 難病ALSの新たな原因遺伝子の発見
(2013/03/12) - 脊髄損傷にヒートショックプロテインが有効?
(2013/03/11) - 片頭痛患者では血管内皮前駆細胞が少ない?
(2013/03/11) - 筋幹細胞の静止状態はmiRNA-489により維持される
(2013/03/11) - ストレスに弱いってどういうこと?(心の病気にかかるメカニズムの一つ、「ストレス脆弱モデル」をネズミで再現)
(2013/03/09) - 核酸医薬は実現するか~筋強直性ジストロフィー治療の可能性~
(2013/03/09) - なくならないのは技がある!
(2013/03/08) - Down症候群のiPS細胞の染色体数を修正する
(2013/03/08) - 高品質なiPS細胞作製のキーファクターZscan4の同定
(2013/03/08) - Turning off the Neuron Death Pathway
(2013/03/07) - 新しい安全な分子標識-マルチ同位体画像質量分析法-が明らかにした幹細胞の不等分裂様式
(2013/03/07) - 重度脊髄損傷後に移植した神経幹細胞が非常に長く軸索を伸長し、シナプス結合した!
(2013/03/07) - 神経系前駆細胞を元気にして水頭症を治す!?
(2013/03/05) - FUS/TLSとTDP-43 二つのALS原因遺伝子の交差点
(2013/03/01) - 貪食細胞マクロファージが造血幹細胞を優しく包み込んで自己複製能の維持に貢献していた!?
(2013/02/27) - TALENs -新遺伝子改変技術が生命科学を変える!?-
(2013/02/27) - RESTタンパク質による遺伝子発現調節 ~遺伝子発現とシナプス機能~
(2013/02/25) - 腸に住んでいるある平凡な細菌によって大腸がんは引き起こされる!
(2013/02/25) - 癌抑制遺伝子p53の変異はメバロン酸経路を活性化することで、正常な乳腺の構造を失わせる
(2013/02/25) - 樹状細胞は制御性T細胞の恒常性をコントロールすることで多発性硬化症を寛解させる
(2013/02/25) - Schwann Cell Plasticity After Spinal Cord Injury Shown by Neural Crest Lineage Tracing
(2013/02/15) - エクソソームは、癌細胞の「飛び道具」!
(2013/02/08) - 老化したニッチでは筋肉幹細胞は静止状態を保てない
(2013/01/31) - 幹細胞を使った創薬開発
(2013/01/31) - 体細胞リプログラミングにおける遺伝子発現調節の解析からわかること-single cellで見てみようの巻-
(2013/01/31) - がん幹細胞発生のかぎを握るのは誰?-ユーイング肉腫がん幹細胞の解析を通じた検証-
(2013/01/31) - 小動物用PET(Positron Emission Tomography)で、ラットの脳梗塞巣を探知することができる [18F]BMS-PET
(2013/01/31) - 脳の神経ネットワークにおけるヤングパワー!
(2013/01/18) - アストロサイトの性格はどうやって決まる?
(2013/01/18) - 幹細胞の自己複製能を制御する因子とは?
(2013/01/18) - アルデヒドが真犯人!?DNA損傷と再生不良性貧血
(2012/12/18) - HIV-2の新しい定量法
(2012/12/18) - Japanese People's Preference for Place of End-of-Life Care and Death: A Population-Based Nationwide Survey
(2012/12/18) - がん細胞の死に際
(2012/12/18) - 癌幹細胞を眠りから目覚めさせる"Coco"
(2012/12/13) - 細胞接着分子のインテグリンが血液の幹細胞の維持を制御する
(2012/12/11) - 移植された神経幹細胞は免疫系にも作用する
(2012/12/11) - 血液がん克服にむけて!~JAK2阻害剤の薬剤耐性メカニズム解明~
(2012/12/04) - 癌進展を陰で操る支配者
(2012/11/30) - 幹細胞の2つの顔を暴け!!! 未分化性維持と特異的分化との狭間で...
(2012/11/30) - 脊髄損傷後の機能回復には自発的なリハビリが効果的
(2012/11/21) - もしあなたの歯が無くなってしまった時に...
(2012/11/15) - iPS細胞から血小板をつくる
(2012/10/30) - メラノーマのエキソソームで予後予測ができる?!
(2012/10/30) - Oligodendroglia Cells Can Do Much More Than an Insulator for Neuron
(2012/09/11) - APJは、心臓肥大のデュアル受容体として作用する
(2012/09/11) - 幹細胞医療;脳梗塞治療への挑戦
(2012/09/11) - 造血幹細胞の老化と若返り
(2012/09/11) - カロリー制限が筋肉を増やす? - トレーニング界の常識に挑戦する新たな"逆説"
(2012/09/11) - 癌幹細胞は治療標的にならない!?
(2012/08/24) - iPS細胞でC型肝炎ウイルス感染のモデルをつくる
(2012/08/09) - ES細胞、iPS細胞から内耳有毛細胞への分化誘導
(2012/08/09) - 造血幹細胞を冬眠させる細胞はなんと神経系の細胞だった!
(2012/07/06) - 個別化治療への障壁 ~多重人格なガンを克服せよ~
(2012/07/06) - 栄養のバランスが新しいニューロンを作り、体重や新陳代謝をコントロールする
(2012/05/11) - 脊髄不全損傷後におこる、残存神経ネットワークの代償機能
(2012/05/11) - "スーパーPTENマウス"
(2012/04/20) - 統合失調症iPS細胞研究が臨床研究になるために
(2012/04/20) - 発癌機序における"はじめの一歩"
(2012/04/06) - iPS細胞は脊髄損傷を治せるのか?
(2012/04/06)
- 大脳皮質の進化の謎に迫る
- 2011年度
- 2010年度
ホーム > 世界の幹細胞(関連)論文紹介 > iPS細胞から血小板をつくる
iPS細胞から血小板をつくる
論文紹介著者

櫻井 政寿(博士課程 3年)
GCOE RA
血液内科
第一著者名・掲載雑誌・号・掲載年月
Takayama N/J Exp Med. 2010 Dec 20;207(13):2817-30.
文献の英文表記:著者名・論文の表題・雑誌名・巻・号・ページ・発行年(西暦)
- Takayama N et al., Generation of functional platelets from human embryonic stem cells in vitro via ES-sacs, VEGF-promoted structures that concentrate hematopoietic progenitors., Blood. 2008 Jun 1;111(11):5298-306.
- Takayama N et al., Transient activation of c-MYC expression is critical for efficient platelet generation from human induced pluripotent stem cells., J Exp Med. 2010 Dec 20;207(13):2817-30.
- Nakamura S et al., Platelet Production System Using An Immortalized Megakaryocyte Cell Line Derived From Human Pluripotent Stem Cells, 2011 53rd ASH Annual Meeting and Exposition #2
- Takayama N et al., Pluripotent stem cells reveal the developmental biology of human megakaryocytes and provide a source of platelets for clinical application. Cell Mol Life Sci. 2012 Apr 24.
論文解説
2006年に発明されたiPS細胞の研究は、現在とても速いスピードで進んでおり、関連するニュースが毎週のように流れています。なぜこれほどまでにiPS細胞は注目されているのでしょう。
現代の医療は大きく進歩しており、肝臓や心臓などの臓器が悪くなった時に、薬や手術で治らなければ、最終手段として「移植医療」があります。しかし移植はドナー(臓器を提供する人)の確保など多くの問題があり、移植を必要とする患者さん全員が受けられる医療ではありません。
それでは人為的に臓器を作り出すことができたら、もっと多くの患者さんが救われるのではないでしょうか。肝臓が悪い人には肝臓をつくり、心臓が悪い人には心臓をつくる――このような医療を総称して「再生医療」と呼びます。そしてiPS細胞は様々な臓器のおおもとの細胞で、育て方次第でいろいろな臓器になる能力を持っています。iPS細胞の発明により、再生医療の実現はすぐそこまで迫ってきているのです。
今回は、主に日本のグループが研究を進め、臨床応用の一歩手前まできている分野について紹介します。
血液を臓器とみなせば、いま日本で最も移植されている臓器は血液です。いわゆる「輸血」です。ご存じのように、輸血は人々の善意から成り立っています。献血センターや献血車を見かけたことがあると思いますが、皆さんが無償で血液を提供してくださることで、救われる患者さんがいます。この美しいシステムにより多くの場合、安全な輸血が実施されていますが、まったく問題がないわけではありません。
一つはやはりドナーの問題です。献血センターにはいつも「ピンチ」と書かれていることが多いと思いますが、献血者は減りつつあります。また稀ではありますが、輸血を介しての感染もゼロではなく、時として社会問題に発展します。
もし人工的に血液を作り出すことができたら、献血に頼らず、感染症の問題のないより安全な輸血が可能となるはず――当然そう考える研究者は以前から存在し、様々なアプローチがなされてきましたが、いまだ実用化には至っていません。しかしここ数年、目覚ましい進歩があり、特に血小板輸血では実用化が見えてきています。
2008年にTakayamaらは多能性幹細胞(ES細胞)を用いて、人工的に血小板を作成することに成功しました1)。しかしこの方法では効率が悪く、1回の輸血製剤をつくるのに、シャーレが何万枚も必要となってしまうため、とても実用化できません。
そこで、Takayamaらは今度はiPS細胞を用いてより効率的な血小板づくりに挑戦しました。複数のiPS細胞からES細胞の時と同じ要領で血小板をつくってみました。その中で、産生効率のよかったiPS細胞を詳しく調べてみると、c-Myc(※1)という遺伝子の活性化が、血小板の前段階の細胞である巨核球の増殖に寄与することがわかりました。それではc-Mycを多く発現させればより効率的に血小板ができるかと思われましたが、話はそう単純ではなく、c-Mycが活性化したままだと、細胞老化誘導因子であるINK4AとARFの発現が上昇し、巨核球が十分に成熟して血小板を放出する以前に、老化して細胞が死んでしまったのです。一方で、最も血小板産生効率の良いiPS細胞ではc-Mycは一時的に活性化するものの、その後発現が低下していました。
この観察結果を裏付けるべく、人為的にc-Mycの発現を上下させてみました。すると、巨核球前駆細胞の段階で一時的にc-Mycの発現を上昇させ、その後低下させた群は、c-Mycが持続的に発現増強した群に比べ、血小板の産生効率が確かに良かったのです2)。
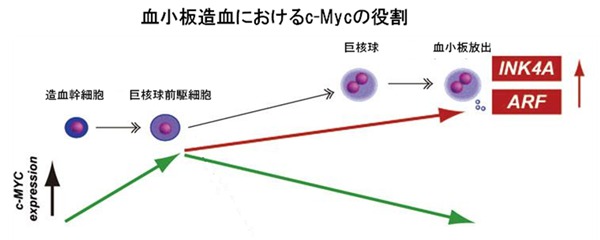
文献4より改変
しかし、この方法でもまだ実用化できるほどの効率を得られません。
そこでNakamuraらは、この方法にさらに改良を加えました。先ほどc-Mycを強く発現させると巨核球が増加するものの、血小板になる前に老化して死んでしまうと書きました。そこで彼らはc-Mycと共にBmi1という遺伝子を強く発現させることでこの問題を解決しました。Bmi1は、先ほど出てきた細胞を老化に導くINK4AとARFを負に制御することで、細胞の老化を防ぎます。そしてc-MycとBmi1を両方強く発現させることで、効率的に血小板を産生し、また老化せず無限に増殖する不死化巨核球細胞株を作成したのです。この方法により、約3週間で1回の輸血相当の血小板を得られるようになりました3)。
様々な臓器で研究が進んでいるiPS細胞による再生医療ですが、臨床応用に際し、最大の課題の一つとなっているのががん化の危険性です。しかし、血小板には核がなく、それ自体では増殖することができないので、がん化の心配性がありません。
輸血の中でも特に血小板輸血は、4日間しか保存しておけないため、安定供給が難しいという面があります。また、頻回の輸血に起因する抗HLA抗体(※2)の産生により、輸血の無効化が起きやすいという問題もありますが、iPS細胞から血小板輸血製剤をつくることができれば、この二つの問題も解決できます。
2012年初めに流れたニュースによれば、これら一連の研究を推し進めている東大・京大のグループは、2015年からの臨床応用を目指しているそうです。いよいよiPS細胞が実用化される日がきます。一人の血液内科医として、またiPS研究に携わる者として、その日を心待ちにしています。
用語解説
- ※1 c-Myc:
もっとも有名ながん遺伝子の1つ。iPS細胞の作製に用いられる「山中因子」の1つでもある(他の3つはOct3/4, Sox2, Klf4)。 - ※2 抗HLA抗体:
HLA(Human Leukocyte Antigen=ヒト白血球抗原)は白血球の血液型と言えるもので、自己と他者の区別に重要な役割を果たす。輸血などで頻回に本人以外のHLA抗原に曝露すると、非自己のHLA抗原に対する抗HLA抗体が出現することがある。それにより患者さんに輸血(特に血小板輸血)をしても、輸血した血液がすぐに患者さんの体内で壊されてしまい、輸血をした意味がなくなってしまうことがある。
Copyright © Keio University. All rights reserved.
