- 2012年度
- 大脳皮質の進化の謎に迫る
(2013/03/29) - 活性型ビタミンDで小胞体ストレスを緩和しよう!
(2013/03/29) - Sweat Glands Grown from Newly Identified Stem Cells
(2013/03/29) - ~筋肉の恒常性と健康は相反するものなのか?~ 筋肉においてオートファジーが存在するが故にインスリン抵抗性が存在する
(2013/03/29) - たった1つの因子の抑制で様々な細胞が神経に!?
(2013/03/28) - 乳酸菌を取り込むと、細胞も若返る?! ~"人間、またしても発酵食品のお世話になる"の巻~
(2013/03/27) - 脳腫瘍における新しい遺伝子変異~エピジェネティク
(2013/03/27) - CCR2-dependentrecruitment of macrophages by tumor-educated mesenchymal stromal cells promotes tumor development and is mimicked by TNFα
(2013/03/25) - 補体C1qはWntシグナルの活性化を介して細胞を老化させる
(2013/03/19) - Speramtogonial Stem Cell Transplantation into Rhesus Testes Regenerates Spermatogenesis Producing Functional Sperm.
(2013/03/12) - 糖尿病薬剤による抗腫瘍効果
(2013/03/12) - 難病ALSの新たな原因遺伝子の発見
(2013/03/12) - 脊髄損傷にヒートショックプロテインが有効?
(2013/03/11) - 片頭痛患者では血管内皮前駆細胞が少ない?
(2013/03/11) - 筋幹細胞の静止状態はmiRNA-489により維持される
(2013/03/11) - ストレスに弱いってどういうこと?(心の病気にかかるメカニズムの一つ、「ストレス脆弱モデル」をネズミで再現)
(2013/03/09) - 核酸医薬は実現するか~筋強直性ジストロフィー治療の可能性~
(2013/03/09) - なくならないのは技がある!
(2013/03/08) - Down症候群のiPS細胞の染色体数を修正する
(2013/03/08) - 高品質なiPS細胞作製のキーファクターZscan4の同定
(2013/03/08) - Turning off the Neuron Death Pathway
(2013/03/07) - 新しい安全な分子標識-マルチ同位体画像質量分析法-が明らかにした幹細胞の不等分裂様式
(2013/03/07) - 重度脊髄損傷後に移植した神経幹細胞が非常に長く軸索を伸長し、シナプス結合した!
(2013/03/07) - 神経系前駆細胞を元気にして水頭症を治す!?
(2013/03/05) - FUS/TLSとTDP-43 二つのALS原因遺伝子の交差点
(2013/03/01) - 貪食細胞マクロファージが造血幹細胞を優しく包み込んで自己複製能の維持に貢献していた!?
(2013/02/27) - TALENs -新遺伝子改変技術が生命科学を変える!?-
(2013/02/27) - RESTタンパク質による遺伝子発現調節 ~遺伝子発現とシナプス機能~
(2013/02/25) - 腸に住んでいるある平凡な細菌によって大腸がんは引き起こされる!
(2013/02/25) - 癌抑制遺伝子p53の変異はメバロン酸経路を活性化することで、正常な乳腺の構造を失わせる
(2013/02/25) - 樹状細胞は制御性T細胞の恒常性をコントロールすることで多発性硬化症を寛解させる
(2013/02/25) - Schwann Cell Plasticity After Spinal Cord Injury Shown by Neural Crest Lineage Tracing
(2013/02/15) - エクソソームは、癌細胞の「飛び道具」!
(2013/02/08) - 老化したニッチでは筋肉幹細胞は静止状態を保てない
(2013/01/31) - 幹細胞を使った創薬開発
(2013/01/31) - 体細胞リプログラミングにおける遺伝子発現調節の解析からわかること-single cellで見てみようの巻-
(2013/01/31) - がん幹細胞発生のかぎを握るのは誰?-ユーイング肉腫がん幹細胞の解析を通じた検証-
(2013/01/31) - 小動物用PET(Positron Emission Tomography)で、ラットの脳梗塞巣を探知することができる [18F]BMS-PET
(2013/01/31) - 脳の神経ネットワークにおけるヤングパワー!
(2013/01/18) - アストロサイトの性格はどうやって決まる?
(2013/01/18) - 幹細胞の自己複製能を制御する因子とは?
(2013/01/18) - アルデヒドが真犯人!?DNA損傷と再生不良性貧血
(2012/12/18) - HIV-2の新しい定量法
(2012/12/18) - Japanese People's Preference for Place of End-of-Life Care and Death: A Population-Based Nationwide Survey
(2012/12/18) - がん細胞の死に際
(2012/12/18) - 癌幹細胞を眠りから目覚めさせる"Coco"
(2012/12/13) - 細胞接着分子のインテグリンが血液の幹細胞の維持を制御する
(2012/12/11) - 移植された神経幹細胞は免疫系にも作用する
(2012/12/11) - 血液がん克服にむけて!~JAK2阻害剤の薬剤耐性メカニズム解明~
(2012/12/04) - 癌進展を陰で操る支配者
(2012/11/30) - 幹細胞の2つの顔を暴け!!! 未分化性維持と特異的分化との狭間で...
(2012/11/30) - 脊髄損傷後の機能回復には自発的なリハビリが効果的
(2012/11/21) - もしあなたの歯が無くなってしまった時に...
(2012/11/15) - iPS細胞から血小板をつくる
(2012/10/30) - メラノーマのエキソソームで予後予測ができる?!
(2012/10/30) - Oligodendroglia Cells Can Do Much More Than an Insulator for Neuron
(2012/09/11) - APJは、心臓肥大のデュアル受容体として作用する
(2012/09/11) - 幹細胞医療;脳梗塞治療への挑戦
(2012/09/11) - 造血幹細胞の老化と若返り
(2012/09/11) - カロリー制限が筋肉を増やす? - トレーニング界の常識に挑戦する新たな"逆説"
(2012/09/11) - 癌幹細胞は治療標的にならない!?
(2012/08/24) - iPS細胞でC型肝炎ウイルス感染のモデルをつくる
(2012/08/09) - ES細胞、iPS細胞から内耳有毛細胞への分化誘導
(2012/08/09) - 造血幹細胞を冬眠させる細胞はなんと神経系の細胞だった!
(2012/07/06) - 個別化治療への障壁 ~多重人格なガンを克服せよ~
(2012/07/06) - 栄養のバランスが新しいニューロンを作り、体重や新陳代謝をコントロールする
(2012/05/11) - 脊髄不全損傷後におこる、残存神経ネットワークの代償機能
(2012/05/11) - "スーパーPTENマウス"
(2012/04/20) - 統合失調症iPS細胞研究が臨床研究になるために
(2012/04/20) - 発癌機序における"はじめの一歩"
(2012/04/06) - iPS細胞は脊髄損傷を治せるのか?
(2012/04/06)
- 大脳皮質の進化の謎に迫る
- 2011年度
- 2010年度
ホーム > 世界の幹細胞(関連)論文紹介 > 癌進展を陰で操る支配者
癌進展を陰で操る支配者
論文紹介著者

樺嶋 彩乃(博士課程 3年)
GCOE RA
内科学(消化器)
第一著者名・掲載雑誌・号・掲載年月
Karen McLean/The Journal of Clinical Investigation Vol.121(8):3206-3219, August 2011
文献の英文表記:著者名・論文の表題・雑誌名・巻・号・ページ・発行年(西暦)
Karen McLean, Yusong Gong, Yunjung Choi, Ning Deng, Kun Yang, Shoumei Bai, Lourdes Cabrera, Evan Keller, Laurie McCauley, Kathleen R. Cho, and Ronald J. Buckanovich.
Human ovarian carcinoma-associated mesenchymal stem cells regulate cancer stem cells and tumorigenesis via altered BMP production. The Journal of Clinical Investigation Vol.121(8):3206-3219, August 2011
論文解説
腫瘍組織は腫瘍細胞とそれを取り巻く細胞である間質細胞と呼ばれる細胞から構成されています。「腫瘍」というと悪性の腫瘍細胞のみが異常増殖しているようなイメージを受けますが、組織型など腫瘍の種類によっては間質細胞の方が組織の大部分を占めているというようなことも少なくありません。治療標的とするべきものは言うまでもなく腫瘍細胞自身ですが、実際は周囲の間質細胞が腫瘍細胞に対して様々な働きかけをし、浸潤・転移など腫瘍の進展に深く関与しているということが治療における大きな障壁となっています。
腫瘍間質細胞となる細胞には多くの種類が存在しますが、中でも「間葉系幹細胞(Mesenchymal Stem Cells: MSC)」※1は近年注目をされている細胞です。しかしながらMSCが腫瘍に対して本当に促進的に働くのかという点については解明の余地が残るところでもありました。そこで本論文で筆者らは健常部由来のMSCに比べて、癌組織由来のMSC(CA-MSC)が腫瘍進展に対しどのような特徴を持つかについて検討を進めました。
1.卵巣癌組織由来のMSCは正常のMSC以上のstemness(stemらしさ、幹細胞としての特徴)を有する
正常のMSCは、骨・軟骨・脂肪へと分化をすることが一つの定義となっています。まず、筆者らは卵巣癌組織由来のCA-MSCがそれぞれへの分化能を有しているということを確認しました。更にこの卵巣癌組織由来のMSCは正常のMSCに比較し、幹細胞としての特徴が優れているということが分かりました。
2.癌組織由来のMSCは癌の形成を促進する
次に筆者らはCA-MSCの腫瘍形成への効果について検討を行いました。卵巣癌細胞単独移植群を対照に、正常組織由来のMSCまたはCA-MSCと癌細胞をそれぞれ共移植した群でマウスの腫瘍形成能を比較したところ、前者では癌細胞単独移植群に比べ腫瘍形成能の促進がほとんど見られなかったのに対し、CA-MSCとの共移植群では腫瘍形成能が著しく亢進していました(Fig.1)。
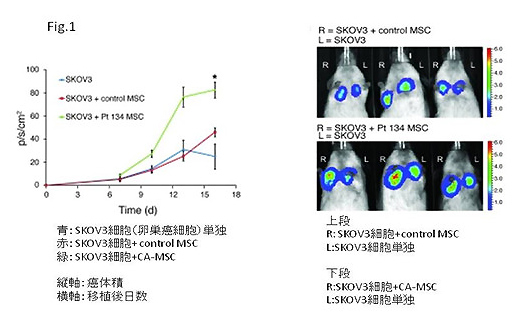
3.卵巣癌組織由来のMSCはBMPシグナルを介して癌幹細胞を制御する
これまで多くの研究により、腫瘍組織中には癌幹細胞と呼ばれる細胞がごく少数の割合で存在することが明らかになっています。それらの細胞は「幹細胞」と表現されるにふさわしく、正常の組織幹細胞と同様に自己複製能を持ち、腫瘍組織を形成します。またこれら癌幹細胞の持つ特徴として、特殊なマーカーの発現や、spheroid(球体)形成能力を有することなどが知られています。
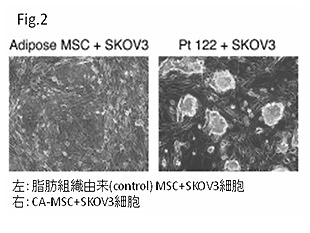
筆者らはCA-MSCが卵巣の癌幹細胞に対してどのように作用するかについても検討を行いました。まず、コントロールの正常組織由来のMSCまたはCA-MSCと卵巣癌細胞とを共培養させました。コントロール群では癌細胞は平面的にしか増殖しなかったのに対し、CA-MSC群では大きな球体を形成しながら増殖していく像を観察することができました(Fig.2)。また、幹細胞特有のマーカーが増加するなど、CA-MSCが癌幹細胞の自己複製能に寄与している可能性が示唆されました。
これまでの検討により、CA-MSCが癌幹細胞に働きかけ癌の進展に対して促進的に作用することが明らかになったので、続いてCA-MSCがどのような分子を発現しているかについて解析を行ったところ、Bone Morphogenetic Protein※2 (BMP)-2,4,6の発現が上昇していることが明らかになりました。そこで、これまでのCA-MSCによる癌促進効果がBMP依存性であったことを示すためにMSCとの共培養に対してBMPの阻害剤であるNogginを作用させたところ、マウスにおける癌形成能が低下し、癌幹細胞の割合の減少が認められました(Fig.3)。以上の結果より、卵巣癌における癌形成促進効果は卵巣癌組織中に存在するMSC由来のBMP依存性である可能性が示唆されました。
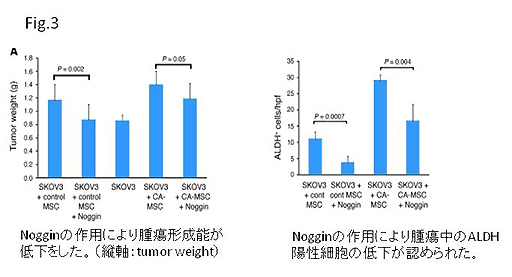
本研究で筆者らは主に脂肪組織や骨髄由来のMSCを正常MSCのコントロールとし、CA-MSCとの比較を行いました。MSCが卵巣癌に対して促進的に作用する過程には、癌組織中において癌細胞由来の何らかの刺激によりCA-MSCと変化することが重要であること、また、このCA-MSCはBMPシグナルを介し卵巣癌幹細胞の進展に寄与することを明らかにしました。癌―間質細胞間におけるシグナルに関しては本研究のBMPシグナル以外にも臓器や細胞によって様々なシグナルの関与が考えられます。根治を目的とした癌治療を考えるうえで、癌幹細胞を標的とする治療が必須となることはこれまで多くの研究により示されてきました。本研究のように、癌幹細胞の動態を司る微小環境の相互作用シグナルを標的とした間接的治療戦略の展開は、癌根治への一つの大きな可能性となるに違いありません。
用語解説
- ※1 間葉系幹細胞:
骨髄・脂肪組織・臍帯など様々な組織に存在する幹細胞であり、骨・軟骨・脂肪などの細胞への分化能を有する。近年では、この細胞を利用し再生医療への貢献が期待されている。また、癌組織へ積極的に動員されることが知られており、癌の研究分野においても近年注目をされている細胞である。 - ※2 BMP(Bone Morphogenetic Protein) :
TGF-βファミリーに属するタンパク質で、標的の細胞に作用し、骨形成を促すだけでなく、細胞増殖・細胞分化・器官発生や形成・アポトーシスなどに関わることが知られている。
Copyright © Keio University. All rights reserved.
