Young Researchers' Trip report
- 2012年度
- 第35回日本分子生物学会年会
(2012年12月13日~2012年12月14日) - Joint 12th International Child Neurology Congress(ICNC)
(2012年5月29日~2012年6月3日) - American Society for Cell Biology (ASCB) 2012 Annual Meeting
(2012年12月15日~2012年12月19日) - 第55回日本甲状腺学会学術集会
(2012年11月29日~2012年12月1日) - 第46回日本小児内分泌学会学術集会
(2012年9月27日~2012年9月29日) - 第35回日本分子生物学会年会
(2012年12月11日~2012年12月14日) - 第35回日本分子生物学会年会
(2012年12月11日~2012年12月14日) - Keystone Symposia : Emerging Topics in Immune System Plasticity
(2013年1月15日~2013年1月20日) - Keystone Symposia : Emerging Topics in Immune System Plasticity
(2013年1月15日~2013年1月20日) - 第35回日本分子生物学会年会
(2012年12月11日~2012年12月14日) - 第35回日本分子生物学会年会
(2012年12月11日~2012年12月14日) - 第35回日本分子生物学会年会
(2012年12月11日~2012年12月13日) - 第35回日本分子生物学会年会
(2012年12月11日~2012年12月14日) - 第35回日本分子生物学会年会
(2012年12月12日~2012年12月14日) - AACR Special Meeting; Tumor Invasion and Metastasis
(2013年1月20日~2013年1月23日) - 浜松ホトニクス 中央研究所 PETセンター
(2012年11月13日~2012年11月29日
(うち5日間)) - 54th ASH (American Society of Hematology) annual meeting
(2012年12月7日~2012年12月15日) - 54th ASH (American Society of Hematology) annual meeting
(2012年12月7日~2012年12月15日) - 54th ASH (American Society of Hematology) annual meeting
(2012年12月7日~2012年12月12日) - 33rd Annual San Antonio Breast Cancer Symposium
(2012年12月4日~2012年12月8日) - Society for Neuroscience 2012
(2012年10月13日~2012年10月18日) - Society for Neuroscience 2012
(2012年10月13日~2012年10月18日) - Society for Neuroscience 2012
(2012年10月13日~2012年10月17日) - Society for Neuroscience 2012
(2012年10月13日~2012年10月18日) - Stanford大学短期留学
(2012年8月20日~2012年9月16日) - BMAP 2012
(2012年8月29日~2012年8月31日) - BMAP 2012
(2012年8月29日~2012年8月31日) - BMAP 2012
(2012年8月29日~2012年8月31日) - BMAP 2012
(2012年8月29日~2012年8月31日) - BMAP 2012
(2012年8月29日~2012年8月31日) - Neuroscience 2012
(2012年9月18日~2012年9月20日(3日間)) - 浜松ホトニクス 中央研究所 PETセンター
(2012年7月24日~2012年8月8日(うち5日間)) - 第14回国際組織細胞化学会議(the 14th International Congress of Histochemistry and Cytochemistry; ICHC 2012)
(2012年8月26日~2012年8月29日) - 共同研究施設訪問:University of Pittsburgh
(2012年9月23日~2012年9月27日) - 第71回日本癌学会学術総会
(2012年9月19日~2012年9月21日) - 第71回日本癌学会学術総会
(2012年9月19日~2012年9月21日) - EMBL Conference: Stem Cells in Cancer and Regenerative Medicine
(2012年8月29日~2012年9月1日) - ISEH (Society for Hematology and stem cells)
(2012年8月23日~2012年8月28日) - 10th International Society for Stem Cell Research 2012
(2012年6月13日~2012年6月16日) - 10th International Society for Stem Cell Research 2012
(2012年6月13日~2012年6月16日) - 10th International Society for Stem Cell Research 2012
(2012年6月13日~2012年6月16日) - 10th International Society for Stem Cell Research 2012
(2012年6月13日~2012年6月16日) - 10th International Society for Stem Cell Research 2012
(2012年6月13日~2012年6月16日) - 10th International Society for Stem Cell Research 2012
(2012年6月13日~2012年6月16日) - 10th International Society for Stem Cell Research 2012
(2012年6月13日~2012年6月16日) - 10th International Society for Stem Cell Research 2012
(2012年6月13日~2012年6月16日) - 10th International Society for Stem Cell Research 2012
(2012年6月13日~2012年6月16日) - 10th International Society for Stem Cell Research 2012
(2012年6月13日~2012年6月16日) - 10th International Society for Stem Cell Research 2012
(2012年6月14日~2012年6月15日) - 10th International Society for Stem Cell Research 2012
(2012年6月13日~2012年6月16日) - 10th International Society for Stem Cell Research 2012
(2012年6月13日~2012年6月16日) - The 58th/ 60th NIBB Conference
(2012年7月17日~2012年7月21日) - Cambridge大学ガードン研究所 留学記
(2011年4月28日~)
- 第35回日本分子生物学会年会
- 2011年度
- 2010年度
ホーム > Young Researchers' Trip report > AACR Special Meeting; Tumor Invasion and Metastasis
AACR Special Meeting; Tumor Invasion and Metastasis
氏名
吉田 剛
GCOE RA
先端医科学研究所遺伝子制御部門
詳細
参加日:2013年1月20日~2013年1月23日
活動レポート
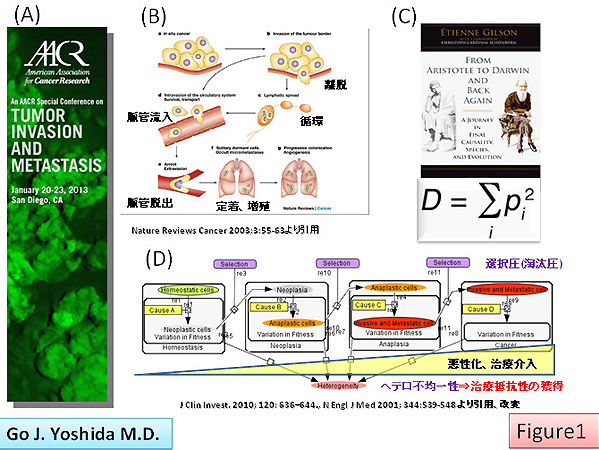
今回僕は幹細胞G-COEのYoung Researcher Support Planに公募し、アメリカ癌学会(AACR; American Association of Cancer Research)がカリフォルニア州のサンディエゴで4日間にわたり主催した、AACR 2013 Special Meeting;Tumor Invasion and Metastasis (Fig1-A)に参加してきました。「腫瘍の浸潤・転移」のみにフォーカスを当てた学術集会とはいえ、EMTや癌幹細胞の概念を提唱した、かの有名なRobert A. Weinberg博士やMichael F. Clarke博士の講演以外にも、300人以上のポスター参加者が非常に活発なdiscussionをしながら進行するinteractiveな学会でした。折しもオバマ米大統領第2期の就任式の時期と重なり、現地21日朝の新聞(USA TODAY)の表紙は"Obama Effect on Race Politics(人種差別克服に対するオバマ大統領の影響力)"でした。CNNをはじめTVのニュースでも連日就任式に関するイベントやニュースが取りあげられていました。また最終日(現地23日)は、海軍サンディエゴ医学研究所(Naval Medical Center San Diego)の創立25周年記念日に相当するそうで、盛り上がりを見せていました。
腫瘍細胞が浸潤・転移する際には複数のステップを要することが知られているため、それぞれの段階における癌細胞やそれを取り巻く微小環境の変化について、数々の研究が世界中で秒進月歩の勢いで進んでいます。原発巣から癌細胞が離脱する(dissociation)、血管内へと侵入する(intravasation)、血管内を癌細胞が循環する(circulation)、前転移ニッチ(pre-metastatic niche)において血管外へと脱出する(extravasation)、そして生着・増殖(colonization and proliferation)して転移巣を形成するという多段階のステップから転移が成立しています(Fig1-B)。特に最近では、癌幹細胞に近い形質を有する上に侵襲性の低い迅速診断に有用であると期待されている血中循環腫瘍細胞(circulating tumor cells; CTC)がますます注目視されつつあります。一般演題発表の参加者や招待講演の先生方の9割以上が乳癌転移モデルやヒト検体を用いた研究であり、癌種やseed and soil theoryの観点からすると、真の意味での腫瘍転移の研究はまだまだ始まったばかりと感じました(http://www.gcoe-stemcell.keio.ac.jp/treatise/2012/20120706_02.html)。
MIHのRichard Hynes博士は"The Extracellular Matrix is Futile Soil."という演題名で講演され、原発巣と転移巣との間で細胞外マトリックス(ECM)成分がどのように変化するのか、そしてその変化を規定しているのは腫瘍細胞なのか、それとも間質細胞なのかをLC/MS-MS解析を用いて明らかにしました。意外にも、大腸癌原発巣と比較して肝転移巣でのみ発現しているECM成分が数多く同定されました。また、Richard博士の共同研究者が、1993年に佐谷先生のもとで『CD44vと転移の関連性』に関してLancet誌に報告した現在マサチューセッツ総合病院で活躍しているK. Tanabe博士であると知った時は、「癌研究の着眼点は無限にあるが、研究者の世間は狭いなぁ」と感じました。
基調講演では、Dana-Farber癌研究所のKornelia Polyak教授が、ダーウィン進化論の観点から乳癌組織のヘテロ不均一性の獲得のメカ二ズムについて解説されました。数理生物学的にShannon Index of Diversity(Fig1-C)で解析したところ、HER2過剰発現乳癌では治療後に8q24染色体異常の腫瘍内ヘテロ不均一性が非常に高まることが明らかになっています。たとえ同じ病理組織型、分化度、そして同一の患者の検体内でも、CD44、CD24、そして染色体欠失や増幅においても異なること、そしてneoadjuvant chemotherapy([例]HER2陽性乳癌患者術前に対するハーセプチン投与)前後でEGFR発現に関する多様性が獲得されることを報告しました。治療前にどれだけのヘテロ不均一性が認められるのか、それが治療応答性や予後を予測するバイオマーカーになるという結論(Fig1-D)でしたが、残念ながら日本では、臨床サンプル研究に対するアクセスの壁が一段と厳しくなっている現状があり、世界の癌研究(systematicな基礎臨床融合型研究)と逆行しているといわざるを得ないと思いました。以前BMC Cancer誌に掲載された『Li-Fraumeni症候群患児における集学的療法によるCD44v発現誘導』に関する論文(http://www.biomedcentral.com/content/pdf/1471-2407-12-444.pdf)でも強調した通り、「真の癌幹細胞」を捉える際には、治療前後での遺伝子発現、エピジェネティック修飾の変化により着眼点を置く必要があると思います。そのためには、もちろん免疫組織染色やマイクロダイセクションだけでなく、様々な手法での解析に耐えられるサンプルが必要になってくると思います。腫瘍細胞がviableかつartifactのストレスがかかっていない状態で、細胞競合・サブクローンの観点から原発巣・転移巣両方を検証するために、臨床サンプルへのaccessibilityを高めていくという必要性があります。
特に興味深かった講演内容を2つほどご紹介したいと思います。
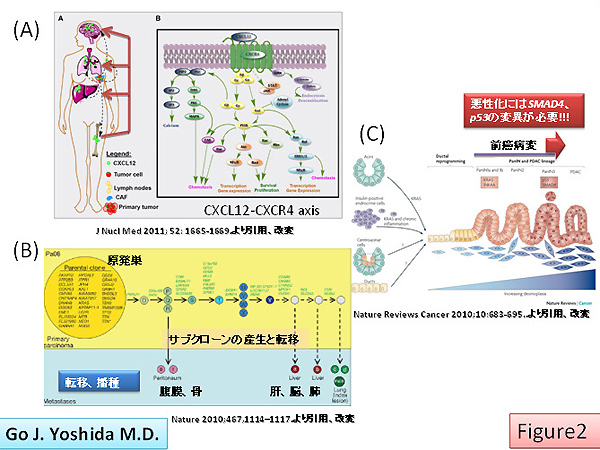
■乳癌の骨転移において従来から破骨細胞(osteoclast)の重要性は指摘されてきましたが、フランスのSylvain Provot博士は低酸素ニッチ(hypoxic niche)における骨芽細胞(osteoblast)の役割について報告されました。VHL遺伝子およびHIF1α遺伝子のコンディショナルノックアウトマウスの解析を通して、VEGF産生による血管新生促進、RANKLを介した破骨細胞の増殖促進などを介して、骨芽細胞は転移を促進することを明らかにしました。興味深かった点は、骨芽細胞が骨転移を促進するだけでなく、原発巣の拡大や他臓器(肺、脳、肝臓など)への転移をも促進する際に、いったん骨に定着した腫瘍細胞がSDF1(CXCL12)-CXCR4 axisを介して活性化され間接的に他臓器に転移するという実験結果でした(Fig2-A)。それとは対照的な講演として、ジョンスホプキンス大学のChristine A. Iacobuzio-Donahue博士の講演のインパクトが高かったです。癌幹細胞の観点から考えた際に、転移の原点(cell-of-origin)となる親株(parental clone)から転移先臓器が異なるごとに、それぞれの臓器の微小環境に適合する多彩なサブクローンが産生される(Fig2-B)という内容でした。癌種や転移を解析するモデルに応じて所見が異なる可能性は大いにありますが、膵癌や大腸癌の多段階での悪性化における遺伝子変異([例]PanINから膵癌に進展する際にSMAD4あるいはp53の変異が必須;Fig2-C)と、遠隔転移におけるサブクローンの新生が酷似しているというChristine博士の考察はやや飛躍している気がしました。既に悪性転化(malignant transformation)を遂げている細胞が有するfounder変異に対して、転移の過程で獲得するprogress変異は転移先臓器によって異なる傾向にあり、個人的には微小環境由来のストレスに適応し選択されたクローンが有するエピジェネティックな修飾が、最終的には転移巣形成の過程で多様性に富むサブクローンの誘導にとって重要であると思いました。加えて、サブクローンが臓器ごとにモノクローナルに転移するのか、それとも混在してポリクローナルに転移するのか(Fig2-B)は今後追及するべき課題かと考えられます。
■Joan Massague博士の講演は"Metastatic Seeding"という演題名で、Fig2-Aでも説明した、骨に存在するDTC(disseminated tumor cell; 播種性腫瘍細胞)がre-seedingを経て他臓器に遠隔転移する現象について詳細に説明されました。Major Question は"How are the metastatic traits are selected that provide no advantage in the primary tumor?"であり、「なぜ自律的に原発巣において転移能を獲得する細胞が出現するのか?」という非常に重要でありながら見落としがちな疑問点を深く考察されました。癌遺伝子によるストレス(oncogenic stress)あるいは化学療法が、TNF-αやIL-6などの炎症性サイトカインを介して腫瘍細胞のCXCL1/2というリガンドの発現を誘導し、その受容体CXCR2を発現しているCD11b+/Gr1+のミエロイド系の間質細胞がケモカインS100A8/9を産生分泌するというpositive feedback機構こそが、parental cloneが転移能を獲得する上で重要です。さらにMDA-MB-231乳癌細胞株内にはSrcシグナルの活性においてヘテロ不均一性が存在し、Src活性が高いクローンを維持しつつ、血清飢餓やIGF1およびCXCL12を加えることでAkt活性が増加するという感受性の高いクローンを樹立したところ、非常に転移能の高い「MDA-231-Cl」という細胞株を新たに樹立し、心腔内投与により形成される骨転移、脳転移巣の解析を進めています。また骨転移では間葉系幹細胞(mesenchymal stem cell; MSC)を教育しCXCL12、IGF-1を多く産生する間質細胞として原発巣に送り出すことで、原発巣と転移巣が互いに協調しながら拡大するというよりも、むしろ、転移巣が原発巣の拡大を誘導するという"metastatic seed pre-selection model"が提唱されていました。会場の質疑応答で「MDA-231-Clの転移能は可逆的なのか?」と質問したところ、「安定的(stable phenotype)であり、転移能は継代しても維持される」との回答でした。骨転移に関与する遺伝子とSrcシグナル関連遺伝子のうち共通する遺伝子群から同定しただけあって、IGF1とCCL12という2つの遺伝子およびそれを分泌するCAF(cancer-associated fibroblast;腫瘍随伴性線維芽細胞)の存在は、転移能を永続的に維持する上でかなり重要な位置にあるようです。
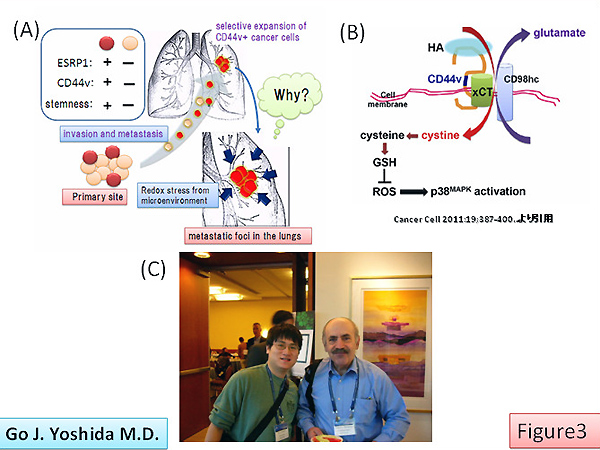
今回の学会発表では、順天堂大学呼吸器内科の八戸博士らが先端研遺伝子制御部門にて明らかにした、乳癌細胞の肺転移における"ESRP1-CD44v-xCT-GSH axis"の重要性(Nat Commun. 2012 Jun 6;3:883., Fig3-A)と論文では掲載されなかった『転移巣におけるCD44vに依存したPI3K/Aktシグナル』、および、『転移巣でNADPHを介して酸化ストレスに富む転移微小環境を誘導するtumor-entrained neutrophil(「腫瘍細胞に教育された好中球」)』に関する未発表データについてポスター発表をしてきました。RNA結合タンパク質であるESRP1(epithelial splicing regulatory protein1)はFGFR2、Mena、p120-catenin、そしてCD44の選択的スプライシング(alternative splicing)を制御することで、多彩なCD44vアイソフォームを産生することが知られています。ESRP1が発現していると酸化ストレス抵抗性を有するCD44v8-10陽性乳癌細胞が誘導され、酸化ストレスや炎症性サイトカインに富む過酷な環境で選択的に生存増殖(selective expansion)することで、結果的に転移巣はCD44v陽性腫瘍細胞で占拠されます(Fig3-A)。たとえESRP1陰性でCD44vを発現していない乳癌細胞を乳腺や尾静脈に移植しても、ほとんど肺には転移巣が形成されません。転移巣における還元型グルタチオン(GSH)とCD44v陽性乳癌細胞の領域が一致し、そのメカニズムとして、CD44vがシスチン輸送体xCTの細胞膜局在を安定化させてGSH合成を促進する点が重要と考えられています(Cancer Cell. 2011;19:387-400., Fig3-B)。CD44v発現に着目した際の腫瘍組織内のヘテロ不均一性が転移巣では酸化ストレスによって失われがちであるという「ボトルネック効果」は、分子標的薬を投与した際にしばしば認められる現象と似ています。関節リウマチや潰瘍性大腸炎の既存薬であるスルファサラジン(SSZ)はxCT阻害作用を発揮することで、"ESRP1-CD44v-xCT-GSH axis"の秩序を破壊することでSSZ投与が従来の抗癌治療と併用することで臨床現場での治療効果を高めると期待されています。既に国内でCD44v発現量や腫瘍内GSH量などをバイオマーカーとして、胃癌患者を対象に治験が進められており、海外の研究者からの注目度はかなり高いものでした。
3日目の午後はRobert A. Weinberg博士の講演があり、偶然にも会場であり滞在先でもあるOmniサンディエゴホテルの学会会場入り口で個人的にお話しすることができました(Fig3-C;右がRobert A. Weinberg博士、左が筆者)。非常に気さくな先生で、日本の大学院生だと自己紹介したところ、「今度のAACRと日本癌学会のJoint Meetingを楽しみにしている」とお答えくださいました。奥様を連れて常に行動していらっしゃり、温かい感じの先生でした。講演でも「自分はSnailやZEBなどのEMT関連転写因子が誘導されていなくても、あくまでどんなシグナルが活性化しても転移が促進されれば、EMTは必ず起きていると信じている」と、ユーモアを交えて熱く語っていました。確かにポスターセッションでも、「E-カドヘリンをノックアウトしただけでβカテニンが遊離して核内に移行して古典的Wntシグナル活性化からEMTが誘導される(もちろんN-カドヘリンがectopicに発現する)」という研究発表もありましたが、4日間の学会を通して、99%の研究者が転移の研究をする際にあまりにも、EMTが起きているか(とりわけTGFβを介したEMTが誘導されているか)に固執しすぎている気がしました。ブレイクスルーになるような研究が期待されます。
東京―サンディエゴ間は直通便がありますが、学会の日程の都合上、行きはサンフランシスコ、帰りはロスを経由しての旅程を組みました。Balboa Parkにあるサンディエゴ動物園や博物館への観光の時間は確保できませんでしたが、折角の好天候に恵まれしたので、チェックインして学会が始まるまでの3時間弱と最終日にチェックアウトしてから飛行場に向かうまでの2時間を使って、歩いて行ける距離にあるSeaport Village(Fig4)で買い物を兼ねて、海岸沿いに散歩をしてきました。Seaport Villageはサンディエゴ湾を望む非常に美しい位置にあるショッピングモール、レストラン、公園ですが、かなり歴史的に古いそうです。タバスコだけを扱った店やシャンプーだけを取りそろえた店やネイティブアメリカンの伝統工芸品を扱った店など非常にユニークな店が立ち並んでいて思わず迷子になってしまいそうでした。ぬいぐるみ専門店があり、思わず愛犬のシーズーにぬいぐるみを3つも買ってしまいました。かつては観光客が来ず廃れた時代もあったようですが、現時点ではその面影は全くなく、地元の人にとっても憩いの場所のようです。最終日にはSeaport Villageからさらに15分ほど歩いたところにあるUSS MIDWAY博物館に行ってきました(Fig5-A)。アメリカ国外では、横須賀港を母港とした最初のアメリカの巨大航空空母であり、内装も充実しており、第二次世界大戦などで使われた様々なタイプの戦闘機、偵察機などが当時の趣をできる限り残しつつ保存されていました(Fig5-B)。MIDWAY博物館に向かう途中には戦争で犠牲になった兵士の名前が掘られた石碑があり、戦争で失われた数々の人命に対する畏敬の念を感じさせる雰囲気も漂っていました(Fig5-C)。音声ガイダンスだけでなく、退役軍人の方々が実際に空母を案内してくださり、当時の空母の様子が窺えました(Fig5-D)。


最後になりましたが、今回の国際学会参加にあたり御指導くださいました先端研遺伝子制御部門佐谷秀行教授ならびに幹細胞G-COEの関係者の皆様に心より御礼申し上げます。
Copyright © Keio University. All rights reserved.
