- 2012年度
- 2011年度
- 新たに判明 がんの転移を促進するメカニズム
(2012/03/23) - 神経発達と加齢における5-hmCを介したエピジェネティクス
(2012/03/23) - TACEを調節するiRhom2は、リステリア菌やLPSの反応により産生されるTNFを制御している
(2012/03/09) - HIV-2って何?
(2012/03/09) - 自殺遺伝子を持ったiPS細胞
(2012/03/09) - リハビリって神経幹細胞も殖やすんです!
(2012/02/24) - 癌幹細胞を制御するHippo pathway
(2012/02/10) - 吸血鬼が若い血を好むのには根拠があった?!~若い生き血でボケ防止~
(2012/02/10) - 癌幹細胞を特異的に標的とした治療法を開発できる可能性!?
(2012/01/27) - 骨の再生には、本来体を守る役割を持つはずのサイトカインは邪魔になる!?
(2012/01/27) - 骨格筋の老化は防げる?
(2012/01/13) - 意外に他力本願???他者の掘ったトンネルを行く癌細胞
(2012/01/13) - 新しいRNA間コミュニケーションのカタチ@筋肉
(2011/12/23) - 精子形成に必須なタンパク質Miwiによるトランスポゾンの発現抑制
(2011/12/23) - Dying well with dementia
(2011/12/09) - Recent insights into the epigenetic regulation of the hair follicle bulge stem cells
(2011/12/09) - ヒトiPS細胞から誘導した神経幹細胞における脳梗塞に対する移植治療の可能性
(2011/11/25) - 体細胞の再プログラム化を阻む"小さなRNA: miR-34"
(2011/11/25) - 薬剤性過敏症症候群 - DIHSがつなぐ薬疹とウイルスとの関連性
(2011/11/11) - 線維芽細胞より作製したドパミン作動性ニューロンは生体内において機能的であるのか?
(2011/11/11) - 終末分化した肝細胞から機能的な神経細胞への直接的な系統転換
(2011/10/28) - Nerves and T Cells Connect
(2011/10/28) - Rapid and robust generation of functional oligodendrocyte progenitor cells
(2011/10/28) - 脂肪細胞が発毛を促進する!?
(2011/10/14) - ADAM13はClass B Ephrinsの分解とWntシグナルの調節により頭部神経冠を誘導する
(2011/10/14) - 多能性の維持に働くchromatin remodeling複合体esBAF
(2011/09/30) - 造血幹細胞の維持にはp57が重要である
(2011/09/30) - IGF-II : 記憶力がよくなる分子!?
(2011/09/16) - 固形腫瘍に存在する間葉系幹細胞は癌幹細胞を増加させる
(2011/09/16) - 小腸は抑制性Th17細胞の宝庫
(2011/09/02) - 細胞周期を制御する新規noncoding RNA
(2011/09/02) - Sema3A play an important role in remyelination failure in multiple sclerosis
(2011/08/19) - Drosophila Sex lethal Gene initiates Female Development in Germline Progenitors
(2011/08/19) - Wnt signaling is a key pathway for regulation of Melanocyte stem cells.
(2011/08/05) - A step closer to understanding the heart
(2011/08/05) - 神経再生を阻む「死」のシグナル
(2011/07/25) - テロメラーゼの再活性化によりマウスの組織老化が回復する
(2011/07/25) - 新遺伝子「Glis1」により、安全なiPS細胞を高効率に作製可能
(2011/07/08) - 幹細胞の"状態"をつくりだす細胞外環境
(2011/07/08) - 毛包幹細胞、色素幹細胞を維持
(2011/06/24) - BCL6を標的とした白血病の新たな治療戦略
(2011/06/24) - 自家移植におけるiPS細胞の免疫応答について
(2011/06/03) - ヒト疾患iPS細胞のウィルソン病への応用
(2011/06/03) - FOP(進行性骨化性線維異形成症)の異所性骨化部の起源は?
(2011/04/22) - 非対称分裂がNotchシグナルの活性化を介して皮膚の分化を促進する
(2011/04/22) - ショウジョウバエの腸管幹細胞の増殖は活性酸素により制御される
(2011/04/22) - 線維芽細胞からの直接的なエピブラストステムセルの誘導
(2011/04/08) - 抗リウマチ薬DHODH阻害剤はメラノーマの進展を抑える
(2011/04/08) - 癌再発の指標になる幹細胞
(2011/04/08)
- 新たに判明 がんの転移を促進するメカニズム
- 2010年度
ホーム > 世界の幹細胞(関連)論文紹介 > 非対称分裂がNotchシグナルの活性化を介して皮膚の分化を促進する
非対称分裂がNotchシグナルの活性化を介して皮膚の分化を促進する
論文紹介著者

松元 芳子(博士課程 3年)
GCOE RA
発生・分化生物学教室
第一著者名・掲載雑誌・号・掲載年月
Scott E. Williams/Nature. 2011 Feb 17;470(7334):353-8.
文献の英文表記:著者名・論文の表題・雑誌名・巻・号・ページ・発行年(西暦)
Asymmetric cell divisions promote Notch-dependent epidermal differentiation.
Williams SE, Beronja S, Pasolli HA, Fuchs E.
Nature. 2011 Feb 17;470(7334):353-8.
論文解説
1. 非対称な細胞分裂がおこる仕組みは?
幹細胞や前駆細胞は、細胞分裂によって、自分と同じ未分化な状態の娘細胞を生み出す(自己複製)か、またはもっと分裂した段階の娘細胞を生じます(分化)。従って、図に示されているように、幹細胞や前駆細胞からの分裂には、同じ種類の娘細胞が2個生み出される対称分裂と1つの幹細胞と1つの分化細胞が生み出される非対称な分裂の大きく2つの分裂様式があります (図1)。
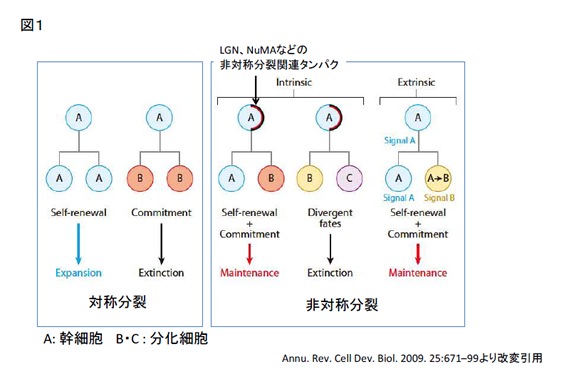
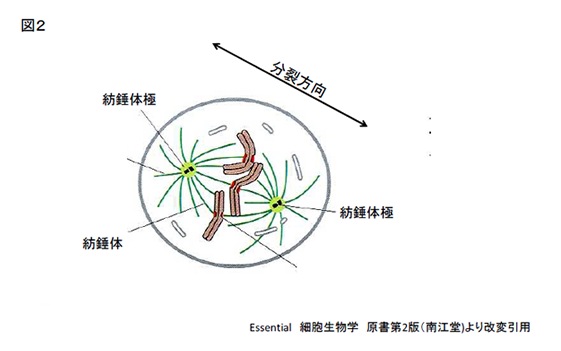
動物の細胞分裂では、ごく簡単には、まず2つの紡錘体極と呼ばれる構造が親細胞の左右(または上下)に分かれていき、ここからのびる紡錘体という細い糸のような構造が細胞の核を両極に引っ張って、核が二つに分かれます。これに続いて、細胞の真ん中にくびれができて、細胞全体が2つに分かれます(図2)。
では、同じ親細胞から性質の異なる2つの娘細胞が生じる非対称分裂はどうして起こるのか、それがこの論文のテーマです。非対称分裂ついては、すでに線虫やショウジョウバエといった非脊椎の実験動物で先行して研究が進められ、細胞分裂の際にLGN、NuMA、Dctn1といったタンパク質が不均等に右と左(または上と下)に分配され、これが2つの紡錘体の向かっていく方向(極性)を決めて非対称分裂につながることが示されてきました。そこで著者らは、これらが脊椎動物であるマウスの皮膚においても非対称分裂を制御しているのかを検討することにしました。
2. LGN、NuMA、Dctn1はマウスの皮膚でも非対称分裂を制御している
マウスでは、胎児期14日目までは皮膚の細胞は単層に並んで水平方向に対称分裂を行います。そして14日目から垂直方向への非対称分裂が始まり、身体の外の方向に向けて分化した皮膚の細胞を生み出しつつ、一番下の層に未分化細胞を残して私達の皮膚のような重層構造を形成していきます。
まず、筆者らは、ShRNAというシステムを使って、LGN、NuMA、Dctn1の遺伝子の発現を胎児期9.5日目の単層皮膚細胞で抑制してみました。そして、胎児16.5日目での単層皮膚細胞の分裂の方向性を確認したところ、コントロールの胎児では大部分の細胞が垂直方向に分裂していた(非対称分裂)のに対し、これら遺伝子のいずれかを発現抑制した場合には、分裂の方向が水平方向(対称分裂)のままになってしまうことが分かりました。
3. 非対称分裂の障害は皮膚の成熟障害につながる
続いて筆者らは、LGN、NuMA、Dctn1のタンパク発現を抑制し単層の皮膚細胞からの非対称分裂が適切に起こらなかった場合の皮膚形成を、皮膚構造が成熟する胎児期17.5-18.5日目において観察しました。すると、これらいずれかのタンパクが発現抑制された場合では、体外の染料が皮膚を容易に通過してしまう状態で、皮膚成熟が適切に行われていないことが分かりました。さらにLGNを発現抑制した上で細かく時間経過を追った観察では、皮膚成熟の障害は胎児期16.5日で既に観察され、生後は脱水のため死亡してしまうことがわかりました。これに加え、LGNは正常では分裂しようとする親細胞の頂点側に三日月上にかたまって局在しますが、こうしたLGNの局在を誘導するタンパクのmInscを単層の皮膚細胞で過剰に発現させたところ、非対称分裂の割合が有意に上昇しさらに成熟皮膚層の厚みも増す、という結果もえられ、非対称分裂と皮膚成熟の密接な関係性が示唆されました。
4. Notchシグナルが皮膚細胞の適切な分化に重要な役割を果たしている
次に、非対称分裂がうまくいかないとどうして皮膚成熟が障害されてしまうのかという点について、筆者らはNotchシグナル経路に着目しました。Notchシグナルとは、ショウジョウバエの神経芽細胞などにおいて、娘細胞の分化を誘導するシグナル経路です。
まず、Notchシグナルに関与するいくつかの遺伝子発現レベルが、最下層の未分化細胞層と、外側に向かって生み出されていく細胞の間で有意に異なることが分かりました。続いて、Notchシグナルが活性化すると蛍光タンパクが発現するように設計されたDNAを胎児期マウスの皮膚細胞に導入したところ、非対称分裂によって外側に向かって生み出された娘細胞では蛍光タンパクが強く発現しNotchシグナルが活性化した一方で、LGNやNuMAを発現抑制した場合には、娘細胞での蛍光タンパクの発現は薄れNotchシグナルが適切に活性化されていないことが分かり、非対称分裂の障害はNotchシグナルの活性化障害と関係があることが分かりました。
5. 非対称分裂がNotchシグナルを活性化する
最後に筆者らは、Notchシグナルの活性化と非対称分裂をコントロールするLGNらタンパクの関係をより丁寧に調べました。そして、Notchシグナルを抑制しても対称・非対称分裂の割合に変化が起こらないこと、LGNの発現を抑制した場合とLGNの発現抑制にさらにNotchシグナルの活性化阻害を組み合わせた場合で、同程度に皮膚の分化障害が生じること、LGNの発現を抑制した場合に生じる皮膚の分化障害をNotchシグナルを強制的に活性化することでかなり正常化できること、の3つの実験結果を得ました。
これらを踏まえ、筆者らは適切な非対称分裂とそれに続いておこる上層細胞側でのNotchシグナルの活性化が皮膚の分化・成熟に重要であると結論づけています。
培養細胞ではなく、マウス胎児の細胞で、分裂機構を解析しているところが非常にインパクトの大きい論文だと思います。本レビューでは割愛しましたが、ShRNAを胎児の単層皮膚細胞に特異的に導入する新しい方法を用いていることも本論文の大きなポイントの1つです。
Copyright © Keio University. All rights reserved.
