- 2012年度
- 2011年度
- 新たに判明 がんの転移を促進するメカニズム
(2012/03/23) - 神経発達と加齢における5-hmCを介したエピジェネティクス
(2012/03/23) - TACEを調節するiRhom2は、リステリア菌やLPSの反応により産生されるTNFを制御している
(2012/03/09) - HIV-2って何?
(2012/03/09) - 自殺遺伝子を持ったiPS細胞
(2012/03/09) - リハビリって神経幹細胞も殖やすんです!
(2012/02/24) - 癌幹細胞を制御するHippo pathway
(2012/02/10) - 吸血鬼が若い血を好むのには根拠があった?!~若い生き血でボケ防止~
(2012/02/10) - 癌幹細胞を特異的に標的とした治療法を開発できる可能性!?
(2012/01/27) - 骨の再生には、本来体を守る役割を持つはずのサイトカインは邪魔になる!?
(2012/01/27) - 骨格筋の老化は防げる?
(2012/01/13) - 意外に他力本願???他者の掘ったトンネルを行く癌細胞
(2012/01/13) - 新しいRNA間コミュニケーションのカタチ@筋肉
(2011/12/23) - 精子形成に必須なタンパク質Miwiによるトランスポゾンの発現抑制
(2011/12/23) - Dying well with dementia
(2011/12/09) - Recent insights into the epigenetic regulation of the hair follicle bulge stem cells
(2011/12/09) - ヒトiPS細胞から誘導した神経幹細胞における脳梗塞に対する移植治療の可能性
(2011/11/25) - 体細胞の再プログラム化を阻む"小さなRNA: miR-34"
(2011/11/25) - 薬剤性過敏症症候群 - DIHSがつなぐ薬疹とウイルスとの関連性
(2011/11/11) - 線維芽細胞より作製したドパミン作動性ニューロンは生体内において機能的であるのか?
(2011/11/11) - 終末分化した肝細胞から機能的な神経細胞への直接的な系統転換
(2011/10/28) - Nerves and T Cells Connect
(2011/10/28) - Rapid and robust generation of functional oligodendrocyte progenitor cells
(2011/10/28) - 脂肪細胞が発毛を促進する!?
(2011/10/14) - ADAM13はClass B Ephrinsの分解とWntシグナルの調節により頭部神経冠を誘導する
(2011/10/14) - 多能性の維持に働くchromatin remodeling複合体esBAF
(2011/09/30) - 造血幹細胞の維持にはp57が重要である
(2011/09/30) - IGF-II : 記憶力がよくなる分子!?
(2011/09/16) - 固形腫瘍に存在する間葉系幹細胞は癌幹細胞を増加させる
(2011/09/16) - 小腸は抑制性Th17細胞の宝庫
(2011/09/02) - 細胞周期を制御する新規noncoding RNA
(2011/09/02) - Sema3A play an important role in remyelination failure in multiple sclerosis
(2011/08/19) - Drosophila Sex lethal Gene initiates Female Development in Germline Progenitors
(2011/08/19) - Wnt signaling is a key pathway for regulation of Melanocyte stem cells.
(2011/08/05) - A step closer to understanding the heart
(2011/08/05) - 神経再生を阻む「死」のシグナル
(2011/07/25) - テロメラーゼの再活性化によりマウスの組織老化が回復する
(2011/07/25) - 新遺伝子「Glis1」により、安全なiPS細胞を高効率に作製可能
(2011/07/08) - 幹細胞の"状態"をつくりだす細胞外環境
(2011/07/08) - 毛包幹細胞、色素幹細胞を維持
(2011/06/24) - BCL6を標的とした白血病の新たな治療戦略
(2011/06/24) - 自家移植におけるiPS細胞の免疫応答について
(2011/06/03) - ヒト疾患iPS細胞のウィルソン病への応用
(2011/06/03) - FOP(進行性骨化性線維異形成症)の異所性骨化部の起源は?
(2011/04/22) - 非対称分裂がNotchシグナルの活性化を介して皮膚の分化を促進する
(2011/04/22) - ショウジョウバエの腸管幹細胞の増殖は活性酸素により制御される
(2011/04/22) - 線維芽細胞からの直接的なエピブラストステムセルの誘導
(2011/04/08) - 抗リウマチ薬DHODH阻害剤はメラノーマの進展を抑える
(2011/04/08) - 癌再発の指標になる幹細胞
(2011/04/08)
- 新たに判明 がんの転移を促進するメカニズム
- 2010年度
ホーム > 世界の幹細胞(関連)論文紹介 > 神経再生を阻む「死」のシグナル
神経再生を阻む「死」のシグナル
論文紹介著者

安田 明正(博士課程 4年)
GCOE RA
整形外科学教室
第一著者名・掲載雑誌・号・掲載年月
Sha Mi/Nat Med (2011) vol. 17 (7) pp. 816-21
文献の英文表記:著者名・論文の表題・雑誌名・巻・号・ページ・発行年(西暦)
Sha Mi1, Xinhua Lee1, Yinghui Hu1, Benxiu Ji1, Zhaohui Shao1, Weixing Yang1, Guanrong Huang1, Lee Walus1, Kenneth Rhodes1, Bang Jian Gong1, Robert H Miller2 & R Blake Pepinsky1. Death receptor 6 negatively regulates oligodendrocyte survival, maturation and myelination. Nat Med vol. 17 (7) pp. 816-21 (2011)
論文解説
多発性硬化症※1・脊髄損傷などの中枢神経の疾患・外傷の治療法に病変部での「髄鞘化」に着目した治療が研究レベルで多く報告されています(※2)。髄鞘とは、ニューロン(神経細胞)の軸索周囲に存在する絶縁性のリン脂質で、絶縁性の髄鞘で軸索が覆われることで、神経線維での信号が円滑に伝導するようになります(図1)。
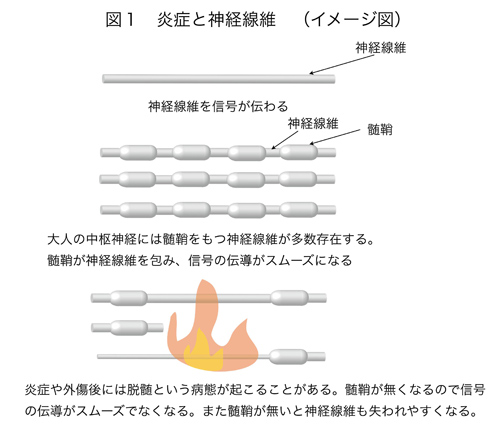
神経線維が髄鞘で覆われることを髄鞘化と呼びます。中枢神経ではオリゴデンドロサイトという細胞が髄鞘を形成しています。また、脳や脊髄が外傷(ケガ)で損傷されたり、炎症などが起こると、様々な障害が起こりますが、その1つに髄鞘が侵される脱髄と呼ばれる状態があります。
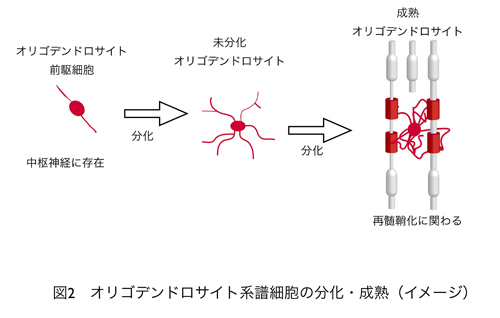
オリゴデンドロサイト前駆細胞※3は脳・脊髄中に存在し、外傷・疾患後には再生の過程でオリゴデンドロサイトへと分化、軸索の髄鞘化(再髄鞘化)を行いますが(※4)(図2)、自然経過では十分な髄鞘化が起こりません。脱髄疾患である多発性硬化症治療の分野では、免疫反応や炎症など病態の一部を治療の対象とした研究は多くされてきましたが、オリゴデンドロサイトの生存・分化に関わる因子には不明な点が多く、直接的にオリゴデンドロサイトの髄鞘化と治療効果を結びつける報告は多くありませんでした。
今回ご紹介する論文は、細胞死受容体(※5)6がオリゴデンドロサイトの生存・成熟・髄鞘化を抑制していることを著者らのグループが発見し、更にはこの受容体の働きを抑えることで脱髄疾患治療に応用できる可能性を見出したという内容のものです。
死の受容体、Death Receptor(以下DR)にはこれまで、DR1からDR6が知られており、これらの受容体が活性化することで細胞に細胞死が誘導されます。最も新しく報告されたDR6が作用する仕組みには不明な点が多く、活性化を促すリガンド(※6)も発見されていませんが、免疫系の維持にも重要であることは分かっていました。
まず、著者らは細胞レベルでの解析でオリゴデンドロサイト系譜の細胞全てがDR6を有し、中でも未分化オリゴデンドロサイトでの発現が強いことを確認しました。そして、オリゴデンドロサイトにおけるDR6の働きを抑制したところ、オリゴデンドロサイトの生存細胞数が増え、更には分化が促進し、成熟オリゴデンドロサイトの細胞数も増加しました。DR6が欠損したノックアウトマウス(※7)から採取したオリゴデンドロサイトにおいても、同様の傾向が確認できました。
続いて著者らは生体内での解析を、ラット及びノックアウトマウスを用いて進めました。一部の髄鞘タンパク質が不足することで起こる疾患がありますが、一方で過剰により引き起こされる疾患もあります。DR6のノックアウトマウスでは、振戦など髄鞘化の異常で起こる症状は確認されていません。さらに、ノックアウトマウスでは生後15日時点での野性型マウスとの比較で髄鞘化が進行していたのに対して、生後30日時点での比較では野性型マウスとは髄鞘化に差は無くなっていたことから、DR6を抑制することで髄鞘化は促進されるものの、過剰な髄鞘化は起こらないことが示唆されました。
次に、多発性硬化症を生じさせたラットにDR6の働きを抑制する抗DR6抗体を投与した研究、およびノックアウトマウスに多発性硬化症を生じさせた研究を行いました。それぞれ、抗DR6抗体を投与したラット及びノックアウトマウスに、良好な機能回復や再髄鞘化が確認でき、DR6を抑制することが脱髄の治療に繋がることが示唆できました。
しかし、多発性硬化症には炎症の関与があり、DR6ノックアウトマウスではT細胞(※8)が病変部で減少することが過去の報告で示されています。従ってこのモデルのみではDR6の抑制によるオリゴデンドロサイト生存の増加や分化の促進が機能回復に寄与したことは示せません(T細胞を抑制した効果によるとも考えられます)。
ここで著者らは、薬品を使用し免疫反応を介さない脱髄モデルをラットおよびノックアウトマウスに作製することで多発性硬化症モデルの際と同様に薬剤投与群およびノックアウトマウスでは早期の再髄鞘化が確認でき、炎症反応の抑制を介さなくても髄鞘化を促進できることが確認できました。
中枢神経の髄鞘を作るのはオリゴデンドロサイトであり、細胞レベルおよび動物実験による研究のいずれにおいてもDR6を抑制することで髄鞘化を促進することができる、ということが本論文での研究で証明されました。
この報告以前は、著者らがLINGO-1という因子がオリゴデンドロサイトの分化を抑制することが示していましたが、炎症細胞への影響は確認されておりません。今回、著者らはDR6の抑制が、病変を悪化させる炎症細胞の増加を防ぎ、更には中枢神経に存在するオリゴデンドロサイト前駆細胞の成熟オリゴデンドロサイトへの分化及び軸索の再髄鞘化を促進することを示して、脱髄疾患治療の糸口になる可能性を見出しました。
手や足などの末梢神経におけるDR6の関与や、損傷後の再髄鞘化は乏しいと言われる老齢の動物においても、DR6の抑制でどの程度の治療効果が期待出来るか、など、この研究に関連して興味は尽きません。
また、軸索を形成するニューロンにもDR6は存在しますが、ニューロンではアミロイド前駆体蛋白質(APP) がDR6のリガンドとなり、細胞死につながることがアルツハイマー病の研究で示されていますが、本研究ではオリゴデンドロサイトの細胞死には関与してないことも示されています。今後の展開には、オリゴデンドロサイトにおけるDR6のリガンドを特定することが肝要であると考えられます。
私は、不明な点を1つ1つ解明していくことが、治療の難しい疾患・外傷への治療に繋がっていくものと信じています。
用語解説
- ※1 多発性硬化症
脳や脊髄などに起こり、様々な神経症状が再発や寛解(症状が落ち着いて安定すること)を繰り返す疾患。脱髄を特徴とする疾患の1つ。免疫反応や炎症が病態に関わるとされる。 - ※2 注釈
脳や脊髄の病気・外傷に神経幹細胞を移植する治療法が検討されているが、幹細胞が分化(細胞が形態を変えて特殊化すること)して「髄鞘化」を行うことも重要だろう、と考えられている。 - ※3 前駆細胞
幹細胞が分化する過程における形態の1つ。ここではオリゴデンドロサイト(分化細胞)は神経幹細胞に由来するが、オリゴデンドロサイト前駆細胞という形態もとる。 - ※4 注釈
髄鞘化は子供成長過程でも起こる。生後、徐々に様々な部位の神経線維に起こっていく。 - ※5 受容体 (英語ではreceptor)
生物の体内に存在し、外界や体内から刺激などを受け取る構造。生物は受け取った刺激を変換し、情報として利用することになる。ここで取り上げた細胞死受容体は特定の刺激を受け取ると、細胞死につながる機構が働くようになっている。 - ※6 リガンド
特定の受容体に特異的に結合する物質のこと。 - ※7 ノックアウトマウス
ある特定の遺伝子が無効化された遺伝子組み換えマウス。特定の遺伝子を不活性化させ、正常のマウスとの比較をすることで、その遺伝子の機能を推定するのに用いることができる。 - ※8 T細胞
免疫系に重要なリンパ球の一種で、中枢神経疾患における炎症にも関与している。
Copyright © Keio University. All rights reserved.
