- 2012年度
- 2011年度
- 新たに判明 がんの転移を促進するメカニズム
(2012/03/23) - 神経発達と加齢における5-hmCを介したエピジェネティクス
(2012/03/23) - TACEを調節するiRhom2は、リステリア菌やLPSの反応により産生されるTNFを制御している
(2012/03/09) - HIV-2って何?
(2012/03/09) - 自殺遺伝子を持ったiPS細胞
(2012/03/09) - リハビリって神経幹細胞も殖やすんです!
(2012/02/24) - 癌幹細胞を制御するHippo pathway
(2012/02/10) - 吸血鬼が若い血を好むのには根拠があった?!~若い生き血でボケ防止~
(2012/02/10) - 癌幹細胞を特異的に標的とした治療法を開発できる可能性!?
(2012/01/27) - 骨の再生には、本来体を守る役割を持つはずのサイトカインは邪魔になる!?
(2012/01/27) - 骨格筋の老化は防げる?
(2012/01/13) - 意外に他力本願???他者の掘ったトンネルを行く癌細胞
(2012/01/13) - 新しいRNA間コミュニケーションのカタチ@筋肉
(2011/12/23) - 精子形成に必須なタンパク質Miwiによるトランスポゾンの発現抑制
(2011/12/23) - Dying well with dementia
(2011/12/09) - Recent insights into the epigenetic regulation of the hair follicle bulge stem cells
(2011/12/09) - ヒトiPS細胞から誘導した神経幹細胞における脳梗塞に対する移植治療の可能性
(2011/11/25) - 体細胞の再プログラム化を阻む"小さなRNA: miR-34"
(2011/11/25) - 薬剤性過敏症症候群 - DIHSがつなぐ薬疹とウイルスとの関連性
(2011/11/11) - 線維芽細胞より作製したドパミン作動性ニューロンは生体内において機能的であるのか?
(2011/11/11) - 終末分化した肝細胞から機能的な神経細胞への直接的な系統転換
(2011/10/28) - Nerves and T Cells Connect
(2011/10/28) - Rapid and robust generation of functional oligodendrocyte progenitor cells
(2011/10/28) - 脂肪細胞が発毛を促進する!?
(2011/10/14) - ADAM13はClass B Ephrinsの分解とWntシグナルの調節により頭部神経冠を誘導する
(2011/10/14) - 多能性の維持に働くchromatin remodeling複合体esBAF
(2011/09/30) - 造血幹細胞の維持にはp57が重要である
(2011/09/30) - IGF-II : 記憶力がよくなる分子!?
(2011/09/16) - 固形腫瘍に存在する間葉系幹細胞は癌幹細胞を増加させる
(2011/09/16) - 小腸は抑制性Th17細胞の宝庫
(2011/09/02) - 細胞周期を制御する新規noncoding RNA
(2011/09/02) - Sema3A play an important role in remyelination failure in multiple sclerosis
(2011/08/19) - Drosophila Sex lethal Gene initiates Female Development in Germline Progenitors
(2011/08/19) - Wnt signaling is a key pathway for regulation of Melanocyte stem cells.
(2011/08/05) - A step closer to understanding the heart
(2011/08/05) - 神経再生を阻む「死」のシグナル
(2011/07/25) - テロメラーゼの再活性化によりマウスの組織老化が回復する
(2011/07/25) - 新遺伝子「Glis1」により、安全なiPS細胞を高効率に作製可能
(2011/07/08) - 幹細胞の"状態"をつくりだす細胞外環境
(2011/07/08) - 毛包幹細胞、色素幹細胞を維持
(2011/06/24) - BCL6を標的とした白血病の新たな治療戦略
(2011/06/24) - 自家移植におけるiPS細胞の免疫応答について
(2011/06/03) - ヒト疾患iPS細胞のウィルソン病への応用
(2011/06/03) - FOP(進行性骨化性線維異形成症)の異所性骨化部の起源は?
(2011/04/22) - 非対称分裂がNotchシグナルの活性化を介して皮膚の分化を促進する
(2011/04/22) - ショウジョウバエの腸管幹細胞の増殖は活性酸素により制御される
(2011/04/22) - 線維芽細胞からの直接的なエピブラストステムセルの誘導
(2011/04/08) - 抗リウマチ薬DHODH阻害剤はメラノーマの進展を抑える
(2011/04/08) - 癌再発の指標になる幹細胞
(2011/04/08)
- 新たに判明 がんの転移を促進するメカニズム
- 2010年度
ホーム > 世界の幹細胞(関連)論文紹介 > 固形腫瘍に存在する間葉系幹細胞は癌幹細胞を増加させる
固形腫瘍に存在する間葉系幹細胞は癌幹細胞を増加させる
論文紹介著者

吉田 剛(博士課程 1年)
GCOE RA
先端医科学研究所 遺伝子制御部門
第一著者名・掲載雑誌・号・掲載年月
Karen McLean/J Clin Invest. 2011 Jul 1. pii: 45273. doi: 10.1172/JCI45273. [Epub ahead of print]
文献の英文表記:著者名・論文の表題・雑誌名・巻・号・ページ・発行年(西暦)
Human ovarian carcinoma-associated mesenchymal stem cells regulate cancer stem cells and tumorigenesis via altered BMP production Karen McLean,1 Yusong Gong,2 Yunjung Choi,2 Ning Deng,2 Kun Yang,2 Shoumei Bai,2 Lourdes Cabrera,1 Evan Keller,3,4 Laurie McCauley,3 Kathleen R. Cho,3 and Ronald J. Buckanovich1,2 1Division of Gynecologic Oncology, Department of Obstetrics and Gynecology, 2Division of Hematology Oncology, Department of Internal Medicine, 3Department of Pathology, and 4Department of Urology, University of Michigan Medical Center, Ann Arbor, Michigan, USA.
論文解説
腫瘍の発生や進展には、腫瘍細胞を取り囲む間質の微小環境が重要な役割を果たすことが数々の研究で証明されてきました。とりわけ腫瘍間質に存在する間葉系幹細胞(mesenchymal stem cell; 以下MSCと略記)が腫瘍の成長・浸潤・転移を促進するのか、それとも抑制するのかに関しては、長年の間、議論の的となってきました。間質微小環境は慢性的な炎症を起こすことで血管新生や腫瘍細胞の浸潤能を増強させるという学説に対して、微小環境が腫瘍細胞の細胞周期をG0期に停止させることで腫瘍の成長を抑制するという学説が存在します。MSCとは中胚葉組織を構成する骨芽細胞、脂肪細胞、軟骨細胞などに多彩に分化する能力を有する未分化な幹細胞であり、細胞表面マーカーとしてCD44、CD73、CD90が重要視されてきました。
本論文では、MSCがどのように固形腫瘍に関与しているのかという命題について、卵巣癌を用いての研究成果を報告しています。まず筆者らは進行期の卵巣癌患者の腹水(注釈1)からCD44、CD73、CD90の抗体とflow cytometryを用いて、卵巣癌に随伴するMSCを単離しました。そして卵巣癌細胞とMSCを共培養することで、MSC自体には腫瘍形成能はなく、また核型も正常であることを確認しました。また正常のMSCと同様に、卵巣癌腹水中のMSCにも骨、脂肪、軟骨に分化する能力があることを免疫染色を用いて証明しました。驚くべきことに幹細胞マーカーであるALDH1(アセトアルデヒド脱水素酵素タイプ1)の酵素活性を解析することで、正常のMSCと比較して卵巣癌腹水中のMSCは「幹細胞らしさ(stemness)」が高度であることが判明しました。実際にALDH1、CD133陽性である癌幹細胞を高率に含むspheroid(浮遊細胞集塊)が散見されました(図1)。
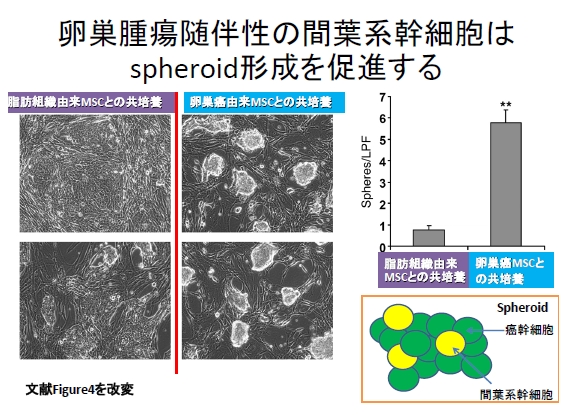
図1
筆者らはさらに、卵巣癌細胞株であるSKOV-IIIと脂肪組織由来MSC、骨髄由来MSC、そして今回の研究で単離した卵巣癌腹水中のMSCとをそれぞれ混合して免疫不全マウスに移植しました。卵巣癌腹水中のMSCの場合は他の2例と比較して3倍以上のサイズの腫瘍が短期間に発症しました。加えて、細胞増殖マーカーであるKi-67発現や血管新生マーカーであるCD31発現が亢進していました。腫瘍組織の一部は脂肪組織や軟骨組織に分化していました。
マイクロアレイ解析という網羅的に遺伝子発現を解析する手法で、卵巣癌腹水中のMSCで発現が亢進している遺伝子を調べたところ、骨形成因子(Bone Morphogenetic Protein:以下BMPと略記)のうちサブタイプ2,4,6が上昇しました。BMPは濃度勾配に従って臓器・組織の発生に関与するmorphogen(モルフォゲン)の一種であり、TGF-βシグナル(注釈2)に影響を与えます。モルフォゲンとは濃度勾配に応じて細胞情報を伝達することで、発生段階などで空間的制御を行う生理物質を指します。具体的にBMP2はNogginを抑制しTGF-βシグナルの転写因子であるSMAD5のリン酸化を促進することで、SMAD5は核内移行して上皮間葉転換(epithelial-mesenchymal transition:以下EMTと略記)を誘導します(図2)。EMTを呈するとALDH1、CD133陽性である癌幹細胞の割合が増加します。癌幹細胞は未分化性を維持しつつ「自己複製能と多分化能」という2つの重要な生物学的性質を備えている細胞です。癌幹細胞は酸化ストレス、慢性炎症、DNA損傷ストレスへの耐性を獲得しています。
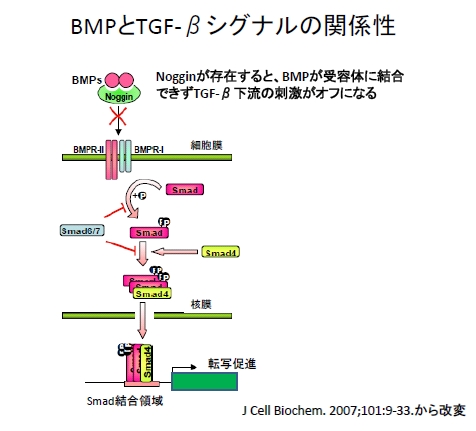
図2
また、臨床検体を用いた研究によって、BMP2発現が亢進している卵巣癌症例の方が予後不良であることが知られています。Nogginを生体内に投与すれば、卵巣癌に随伴する間葉系幹細胞におけるTGF-βシグナルを抑制することで、EMTを抑制するばかりでなく、癌幹細胞の増加を防ぐことができると考えられます。癌幹細胞は外科摘出・化学療法・放射線療法後の微小残存病変(minimal residual disease: MRD)に由来する再発や遠隔転移の責任細胞であることから、本論文は癌幹細胞に標的を絞った新規治療で腫瘍随伴性間葉系幹細胞が重要であることを強く示唆するインパクトのある研究成果と言えます。
注釈
- 腹水
卵巣腫瘍に最もよく起こる転移形式は腹膜播種(種を蒔くように癌細胞が腹膜を広がっていく転移)です。腹膜播種が進むと腹水が貯留してきます。腹水中には数多くの癌幹細胞が浮遊していることが知られています。最近、腹水を伴う進行期の卵巣癌に対して抗EpCAMと抗CD3抗体を含むカツマキソマブ(Catumaxomab;商品名レモマブ、Remomab)の有用性が注目されています(図3)。
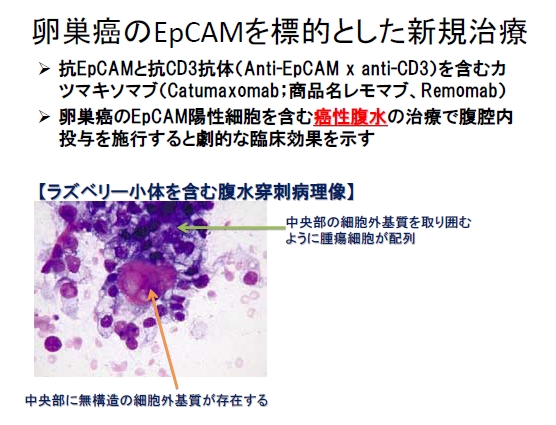
図3
- TGF-βシグナル
細胞増殖の制御や分化、発達において重要な役割を果たすシグナル伝達です。一般的に、リガンドにより惹起されるセリン/スレオニン受容体キナーゼの多量体形成と、BMP経路については Smad1/5/8 といった細胞内シグナル分子のリン酸化によって、また、TGF-β/アクチビン経路については Smad2/3 のリン酸化によってシグナルが活性化します。腫瘍発生初期には細胞増殖を抑制し、腫瘍が進展すると逆に細胞増殖を促進するという二面性を持っています。癌幹細胞との関連でみますと、脳腫瘍ではTGF-βシグナルは癌幹細胞を増加させますが、スキルス胃癌では減少させるといったことが報告されており、残念ながら一元的には関連性を説明できません。
Copyright © Keio University. All rights reserved.
