- 2012年度
- 2011年度
- 2010年度
- 骨髄由来の筋繊維芽細胞は間葉系幹細胞のニッチの構築と腫瘍増殖を促進する
(2011/03/25) - リプログラミングを促進する小さなRNA
(2011/03/25) - ⊿Np63は転写因子Lshを介して、がん幹細胞の増加を促す
(2011/03/25) - 造血幹細胞のメンテナンスを行う新たな因子の発見
(2011/03/04) - マウスES細胞から神経細胞への分化を方向づける因子の発見
(2011/03/04) - ヒト疾患iPS細胞:自閉症レット症候群への応用
(2011/02/18) - 生きかえる心臓
(2011/02/18) - グリオブラストーマ幹細胞様細胞は内皮細胞へ分化し、血管新生を誘導する
(2011/02/04) - 血液の幹細胞を保存状態と臨戦態勢に分類するNカドヘリン
(2011/02/04) - 急性骨髄性白血病のがん幹細胞への集中的治療を可能にするTIM-3
(2011/01/21) - p53の機能の回復を対象とした、がんの治療法には限界がある?
(2011/01/21) - 前立腺癌は分泌細胞、基底細胞のどちらに由来するのか?
(2011/01/07) - 癌細胞をリプログラミングする
(2011/01/07) - 造血幹細胞のエネルギー代謝や恒常性は、Lkb1によって調節される
(2010/12/24) - G-CSFによる造血幹細胞の末梢血への動員がEGFRシグナルの阻害により増強される
(2010/12/24) - 恐竜は何色?
(2010/12/10) - ヒト胚性幹細胞から軟骨細胞への分化誘導
(2010/12/10) - ヒト皮膚細胞から人工造血細胞への驚くべき変換
(2010/11/26) - ただ一つの遺伝子をヒトの皮膚細胞に導入し血液のもとになる細胞を作り出すことに成功
(2010/11/26) - TAp63のDicerを介した転移抑制機構
(2010/11/12) - ヒト細胞における、エンハンサー的機能をもつ長鎖ノンコーディングRNAの発見
(2010/11/12) - 毛包の前駆細胞から生じるSKPs(皮膚由来多能性前駆細胞)は、成人真皮幹細胞としての特性を示す
(2010/10/29) - X染色体上の遺伝子発現を正常化させると、体細胞クローン胚の生産効率は著しく向上する
(2010/10/29) - miR-9は乳癌においてE-cadherinの発現を抑制し、癌転移を促進する
(2010/10/15) - 間葉系幹細胞と造血幹細胞が形成する独特な骨髄ニッチ
(2010/10/15) - 細胞運命決定因子Musashiによる白血病の制御
(2010/10/01) - 単一のLgr5幹細胞からのin vitroでの陰窩・絨毛構造の構築
(2010/10/01) - 造血幹細胞は、インターフェロンγによって活性化される
(2010/09/17) - iPS細胞に残る由来細胞の記憶
(2010/09/17) - 生後の海馬の神経新生は、記憶(恐怖連合記憶)の情報処理(海馬依存的な期間)を制御する
(2010/09/03) - 核質に存在するヌクレオポリンは発生と細胞周期に関連する遺伝子の発現に直接的に関与している
(2010/09/03)
- 骨髄由来の筋繊維芽細胞は間葉系幹細胞のニッチの構築と腫瘍増殖を促進する
ホーム > 世界の幹細胞(関連)論文紹介 > p53の機能の回復を対象とした、がんの治療法には限界がある?
p53の機能の回復を対象とした、がんの治療法には限界がある?
論文紹介著者

稲川 悠紀(博士課程 1年)
GCOE RA
先端医科学研究所遺伝子制御研究部門
第一著者名・掲載雑誌・号・掲載年月
David M. Felder/Nature, 468: 572-576
文献の英文表記:著者名・論文の表題・雑誌名・巻・号・ページ・発行年(西暦)
Stage-specific sensitivity to p53 restoration during lung cancer progression
David M. Feldser, Kamena K. Kostova, Monte M. Winslow, Sarah E. Taylor, Chris Cashman, Charles A. Whittaker, Francisco J. Sanchez-Rivera, Rebecca Resnick, Roderick Bronson, Michael T. Hemann & Tyler Jacks
Nature, 468: 572-57
論文解説
昨年のNatureに、p53遺伝子を対象としたがんの治療法について一考を要する論文が掲載されました。今回の論文紹介では、この論文を取り上げさせていただきます。
p53遺伝子に関する研究は、新聞やニュースでもよく取り上げられることがあるため、耳にしたことがあるという方も多いかもしれません。今回は、まずp53遺伝子について知っていただき、その後、取り上げた論文を紹介いたします。
<p53の働き>
がんは、遺伝子に突然変異が起こり、がん化を引き起こす遺伝子(がん遺伝子)の出現することや、がん化を防ぐ重要な遺伝子(がん抑制遺伝子)の働きが失しなわれることが積み重なって、細胞が異常な増殖を始めることにより発生すると考えられています。今回紹介する『p53』という遺伝子は、がん抑制遺伝子の中で最も有名な遺伝子の1つで『ゲノムの守護神』とも呼ばれています。
細胞は常に様々な刺激を受けていますが、p53は刺激に応じて他の遺伝子を働かせることで、守護神の名の通り、DNAの傷の修復に関与したり、細胞の分裂(細胞周期)の調整を行ったりします。傷が修復できないほど深い場合には、アポトーシス(*1)を誘導し、異常な細胞の排除を促すという働きも担っています。例えるなら、p53の働きとは『正常な細胞を守る為の司令塔であり、その役割を果たす為に、様々な部署に的確な指示を送っている』というイメージです。(図1)
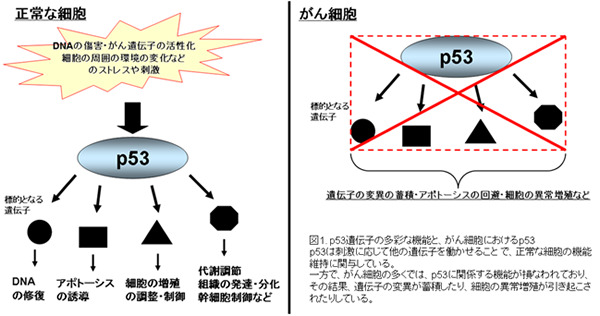
近年ではp53が組織の形成や、組織幹細胞の制御に関与している知見も得られています。2009年には、iPS細胞の作製効率に、p53を介した働きが関与していたことが報告されました。これまでのがん研究で得られた知見とiPS細胞の分野がリンクした、とても興味深い話でした。
<p53はがん治療のよい標的?>
正常な細胞の維持に大事な役割を果たしているp53ですが、『多くのがんにおいて、p53の働きは失われていること』が明らかになっています。このため、p53の関連する機能を、薬剤等を用いて回復させることで、がんの有効な治療法とする研究がこれまでに行われています。
今回、Feldserらのグループは、Kras(*2)の遺伝子変異により肺がんを形成するモデルマウスを作製し、『p53の機能を回復させた時に見られる治療効果』について、検討を行いました。
肺がんが形成されたマウスに対し、p53の機能を回復させると、腫瘍の縮小が観察されました。また、p53の機能の回復により、がん組織において、細胞の増殖を制御する機構が回復している結果も得られました。
がん組織に対して抑制効果がみられた結果から、p53の機能回復は効果的だ!めでたし、めでたし・・・と思いたいところですが、1つ1つのがんをよくよく観察してみると、p53の機能回復の影響がそれぞれのがん組織で異なっていることにFeldserらは気付きました。また、悪性度の高いがんが形成されるよりも前の早い時期からp53の機能を回復させた場合では、効果に大きな違いが見られませんでした。これらの結果から、Feldserらは『一部の悪性度の高いがん細胞だけが、p53の影響をよく受けているのではないか?』と仮説を立て、より詳しい解析を続けました。
<p53の機能回復の効果の違いは?>
p53の機能回復の影響の違いは、どういう働きにより生じているのでしょうか?
Feldserらはまず、がん化を進める機構に注目し、悪性度が高いがん細胞と、そうでないがん細胞の違いを調べました。
その結果、『Kras遺伝子の働きが悪性度の高いがんで顕著に高いこと』を見出しました。また、Kras遺伝子が増幅する変異も観察され、Kras遺伝子以外にも、悪性度の高いがん細胞ではがん化に関する複数の遺伝子の活性化も見られました。 一方で、悪性度の低いがん組織においては、このような特徴は見られませんでした。
では、悪性度の高いがん細胞で見られたKras遺伝子の活性化と、p53の回復効果に、どのような関係があるのでしょうか?
これまでの研究から、『Kras遺伝子の働きが強くなることで、Arf(*3)という遺伝子の働きが強くなる』ことが示されています。この『Arfの働きとしては、p53の働きを促す役割、p53にとっては上司にあたるような役割を持つこと』が知られています。
実際にKras遺伝子の働きが強い、悪性度の高いがん細胞においては、Arfの遺伝子の働きも強くなっていることが観察されました。そして、Arfの遺伝子の働きを抑えてしまうと、p53の機能を回復させたときの効果が弱い結果も得られました。
<今回の論文のまとめ>
Kras遺伝子の変異による肺がんモデルマウスを用いた解析の結果をまとめると、
- 悪性度が高いがん組織では、Kras遺伝子をはじめとするがん化を進展させる遺伝子の働きが強くなっており、これによりArf遺伝子の働きが強くこと。
- このArfの働きが強い組織では、p53の機能回復の効果がより発揮されることが示されました。
- 一方で、悪性度の高くない組織では、Arfの働きが弱く、p53の機能回復の効果が見られませんでした。
Feldserらはこれら結果より、『p53の機能回復は悪性度の高いがん組織でのみ効果を示し、不完全ながんの縮小を示す可能性があること』。また、がん組織の1部が残ってしまうことから『抗がん治療において、p53の機能回復だけでは限界があるのでは?』という考えを提示しています。(図2)
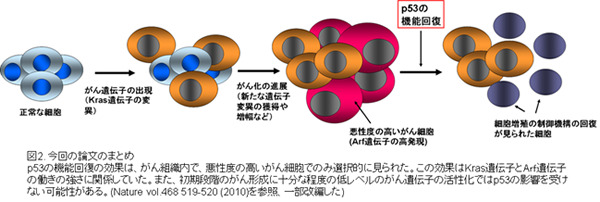
<最後に>
今回の報告から、中には「p53を対象とした治療法はダメなのか・・・」と思う方もいらっしゃるかもしれません。
確かに、p53だけでは、完全にがんをなくすことが出来ない為、不完全でした。しかし、悪性度の高いがん細胞には十分に効果的な結果が示されていました。p53だけではなく、他の遺伝子などを対象とした治療法と併せることで、よりよい治療法が生まれるのではないでしょうか?そのためには、がん化の発生する機構の解明をはじめとした基礎的な研究がまだまだ必要とされるでしょう。
また、このような基礎研究は、他の研究分野に貢献することもあります。たとえば、先ほど紹介したiPS細胞の樹立効率を上昇させるために、p53の働きを研究し得られた知見が役に立つこともあるかもしれません。
p53という有名人を私のようなものが紹介させていただくのは恐縮でしたし、拙い記事でしたが、p53をはじめ、研究のことなどに少しでも興味を持って頂ければ幸いです。また、小さいことの1つ1つの積み重ねや、先人の素晴らしい研究が合わさって、新たな知見が得られていくという研究の1面を感じていただければ、と思います。
解説
- *1 アポトーシス・・・細胞自身により調整・管理された細胞死のこと。多細胞生物において見られる現象で、組織の発生・形成時や、正常な組織を保つ為に引き起こされる。
- *2 Kras・・・Rasと呼ばれる遺伝子ファミリーの1つ。増殖因子などの刺激を受けて、他の遺伝子の働きを促し、正常な細胞においては、増殖などに関与すると考えられている。膵臓がんや大腸がん、肺がんなどのがんにおいては、変異が生じており、常に他の遺伝子の働きを促して、異常な細胞増殖などに寄与していると考えられている。
- *3 Arf(p14)・・・p53のタンパク分解を抑制し、p53の活性化に寄与することで、細胞老化やアポトーシスを誘導に関与すると考えられている遺伝子。
Copyright © Keio University. All rights reserved.
