- 2012年度
- 2011年度
- 2010年度
- 骨髄由来の筋繊維芽細胞は間葉系幹細胞のニッチの構築と腫瘍増殖を促進する
(2011/03/25) - リプログラミングを促進する小さなRNA
(2011/03/25) - ⊿Np63は転写因子Lshを介して、がん幹細胞の増加を促す
(2011/03/25) - 造血幹細胞のメンテナンスを行う新たな因子の発見
(2011/03/04) - マウスES細胞から神経細胞への分化を方向づける因子の発見
(2011/03/04) - ヒト疾患iPS細胞:自閉症レット症候群への応用
(2011/02/18) - 生きかえる心臓
(2011/02/18) - グリオブラストーマ幹細胞様細胞は内皮細胞へ分化し、血管新生を誘導する
(2011/02/04) - 血液の幹細胞を保存状態と臨戦態勢に分類するNカドヘリン
(2011/02/04) - 急性骨髄性白血病のがん幹細胞への集中的治療を可能にするTIM-3
(2011/01/21) - p53の機能の回復を対象とした、がんの治療法には限界がある?
(2011/01/21) - 前立腺癌は分泌細胞、基底細胞のどちらに由来するのか?
(2011/01/07) - 癌細胞をリプログラミングする
(2011/01/07) - 造血幹細胞のエネルギー代謝や恒常性は、Lkb1によって調節される
(2010/12/24) - G-CSFによる造血幹細胞の末梢血への動員がEGFRシグナルの阻害により増強される
(2010/12/24) - 恐竜は何色?
(2010/12/10) - ヒト胚性幹細胞から軟骨細胞への分化誘導
(2010/12/10) - ヒト皮膚細胞から人工造血細胞への驚くべき変換
(2010/11/26) - ただ一つの遺伝子をヒトの皮膚細胞に導入し血液のもとになる細胞を作り出すことに成功
(2010/11/26) - TAp63のDicerを介した転移抑制機構
(2010/11/12) - ヒト細胞における、エンハンサー的機能をもつ長鎖ノンコーディングRNAの発見
(2010/11/12) - 毛包の前駆細胞から生じるSKPs(皮膚由来多能性前駆細胞)は、成人真皮幹細胞としての特性を示す
(2010/10/29) - X染色体上の遺伝子発現を正常化させると、体細胞クローン胚の生産効率は著しく向上する
(2010/10/29) - miR-9は乳癌においてE-cadherinの発現を抑制し、癌転移を促進する
(2010/10/15) - 間葉系幹細胞と造血幹細胞が形成する独特な骨髄ニッチ
(2010/10/15) - 細胞運命決定因子Musashiによる白血病の制御
(2010/10/01) - 単一のLgr5幹細胞からのin vitroでの陰窩・絨毛構造の構築
(2010/10/01) - 造血幹細胞は、インターフェロンγによって活性化される
(2010/09/17) - iPS細胞に残る由来細胞の記憶
(2010/09/17) - 生後の海馬の神経新生は、記憶(恐怖連合記憶)の情報処理(海馬依存的な期間)を制御する
(2010/09/03) - 核質に存在するヌクレオポリンは発生と細胞周期に関連する遺伝子の発現に直接的に関与している
(2010/09/03)
- 骨髄由来の筋繊維芽細胞は間葉系幹細胞のニッチの構築と腫瘍増殖を促進する
ホーム > 世界の幹細胞(関連)論文紹介 > ただ一つの遺伝子をヒトの皮膚細胞に導入し血液のもとになる細胞を作り出す...
ただ一つの遺伝子をヒトの皮膚細胞に導入し血液のもとになる細胞を作り出すことに成功
論文紹介著者

山下 真幸(博士課程 1年)
GCOE RA
発生・分化生物学
第一著者名・掲載雑誌・号・掲載年月
Eva Szabo/Nature, Published online 07 November 2010
文献の英文表記:著者名・論文の表題・雑誌名・巻・号・ページ・発行年(西暦)
Eva Szabo, Shravanti Rampalli, Ruth M. Risueño,Angelique Schnerch, Ryan Mitchell, Aline Fiebig-Comyn, Marilyne Levadoux-Martin and Mickie Bhatia. Direct conversion of human fibroblasts to multilineage blood progenitors. Nature Published online 07 November 2010
※2010/11/26更新分は、2人の大学院生が同一の論文を取り上げました。同じ論文を取り上げても、それぞれの興味や立場によって切り口も異なります。そういった多様性を感じながらお読みいただければと思います。
論文解説
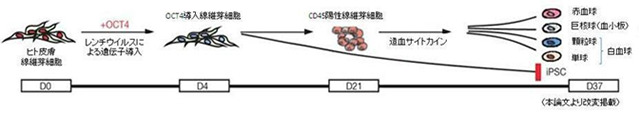
ただ一つの遺伝子「Oct4」をヒトの皮膚から得られた線維芽細胞(※1)に組み込むことにより、様々な種類の血液細胞を生み出すことのできる造血前駆細胞(※2)が生じることを、カナダの研究チームが発見しました。
患者自身の細胞から別の組織の細胞を作ることを考えた場合、まず線維芽細胞から様々な組織の細胞に変化する能力を持つiPS細胞(※3)を作り、そこから目的とする組織の細胞を間接的に作り出す手法が一般的です。しかしその仕組みは複雑で、目的の細胞だけを効率よく作り出すことはなかなか難しいのが実情でした。今回の発見は、ヒトの線維芽細胞に遺伝子OCT4を導入するとiPS細胞を経由せずに血液細胞ができたという画期的なもので、これによりヒトの線維芽細胞から血液細胞を直接作り出す道が開かれました。iPS細胞を用いる手法に比べシンプルでより安全と考えられ、今後の臨床応用が期待されています。
今回の発見はどのような経緯でなされたのでしょうか。筆者らは、線維芽細胞からiPS細胞を作る際、iPS細胞になりきれなかった細胞に注目すると、血液細胞の指標であるCD45というタンパク質を発現する集団があることに気付きました。この集団では特に遺伝子OCT4の働きが高くなっており、SOX2やNANOGといったiPS細胞に特徴的な他の遺伝子の働きは対照的に低くなっていました。そこで筆者らは、この集団がOCT4の働きによって生まれたのではないかと考え、線維芽細胞にウイルスを用いてOCT4を導入する実験を行ったところ、OCT4を導入した線維芽細胞(OCT4導入線維芽細胞)の中にCD45を発現している集団(CD45陽性線維芽細胞)があることがわかりました。これらの細胞の遺伝子発現パターンをみてもiPS細胞に特徴的な遺伝子の働きは変化しておらず、免疫不全マウスに移植してもiPS細胞のように奇形腫(※4)を作りませんでした。これらのことから、OCT4を線維芽細胞に導入するとiPS細胞を経ずに直接CD45陽性線維芽細胞を作れるということがわかりました。
では、このCD45陽性線維芽細胞は本当に血液細胞としての機能を持っているのでしょうか。筆者らはCD45陽性線維芽細胞にサイトカイン(※5)と呼ばれる様々な刺激因子を加えて培養し、成熟した血液細胞ができるかどうかを調べました。すると驚くことにリンパ球を除くすべての白血球、赤血球、血小板に変化できることがわかりました。特に赤血球についてはiPS細胞から作った場合と違って大人の赤血球と同じタイプのヘモグロビンを持っており、これは将来輸血などの臨床応用を考える上で重要と考えられました。さらに、このCD45陽性線維芽細胞を免疫不全マウスに骨髄移植したところ、臍帯血に匹敵する生着率を示し、この細胞が前駆細胞としての性質をもっていることがわかりました。つまり、OCT4を導入することによってリンパ球を除くすべての血液細胞に変化できる造血前駆細胞を作ることができた、ということが証明されたのです。
筆者らはその分子メカニズムに迫るため、OCT4を導入してから時間が経過するにつれて遺伝子の働きがどのように変化していくかを調べました。その結果CD45陽性細胞が出現するにつれて、線維芽細胞に特徴的な遺伝子の働きは低下していき、逆に造血に関わる遺伝子の働きが活発になっていくことがわかりました。さらにOCT4導入細胞で働きの高かった遺伝子のプロモーターやエンハンサー(※6)領域にはOCT4が多く結合し、逆に造血に関係のない遺伝子や多能性に関わる遺伝子ではOCT4はほとんど結合していないこともわかりました。以上のことから、OCT4は造血に関わる様々な遺伝子に同時に働きかけ、線維芽細胞を造血前駆細胞に変化させることが示唆されました。
今回の研究成果は大変センセーショナルで、様々な場面での応用も期待できる画期的な発見といえますが、これをすぐに臨床応用できるというわけではありません。実際にヒトの体内に入った場合に有害な副作用が起きないかどうかなど、検証しなければならない課題は多く残されています。
しかしながら今回の発見は、患者自身の皮膚細胞から目的の細胞を直接作り出し、それを治療に応用するという細胞療法の新たな手法の足がかりになると期待されます。たった一つの遺伝子の働きによって線維芽細胞から造血前駆細胞という全く性格の異なる細胞に変化していくという今回の知見は、臨床応用の可能性のみならず、全ての血液細胞のおおもとである造血幹細胞の起源を考える上でも非常に興味深いと考えます。造血幹細胞の起源はまだはっきりとはわかっていませんが、ひょっとすると同じようなことが生体内でも起こっているのかもしれません。今後の研究の進展が楽しみです。
用語解説
- ※1 線維芽細胞
皮膚をはじめとする様々な組織に存在し、コラーゲンやエラスチンといったタンパク質を分泌する細胞。皮膚の機能を保つために最も重要な細胞とされ、細胞と細胞の間にある隙間(細胞外マトリックス)を維持する働きや、傷ができたときにその近くに移動し隙間を埋める役割を担っている。 - ※2 造血前駆細胞
いくつかの種類の血液細胞に変化できる細胞のこと。全ての血液細胞に変化できる造血幹細胞は、この造血前駆細胞を経て白血球や赤血球、血小板といった成熟細胞に変化すると考えられている。造血前駆細胞はいくつかの段階が知られており、各段階で変化できる細胞の種類が異なっている。 - ※3 iPS細胞(induced pluripotent stem cells; 人工多能性幹細胞)
主に皮膚の線維芽細胞に遺伝子を導入することによって、自分と同じ細胞を複製する能力と、神経や心臓など様々な組織の細胞に変化する能力を新たに備えた細胞のこと。本文に登場するOCT4, SOX2, NANOGはいずれもiPS細胞樹立の際に導入される遺伝子として一般的である。 - ※4 奇形腫
外胚葉(皮膚や神経など)、中胚葉(骨や心臓、血液など)、内胚葉(胃や小腸、肝臓など)のうち複数の成分を持つ腫瘍のこと。iPS細胞を免疫能力のないマウスに移植すると、この三胚葉全ての成分をもった奇形腫ができることが知られている。逆に、この現象をiPS細胞の持つ様々な組織に変化できる能力の証拠とする場合が多い。 - ※5 サイトカイン
主に免疫に関わる細胞から分泌され、増殖や成熟、運動といった様々な刺激を他の細胞に対して与える因子。細菌に感染すると白血球が増えたり、貧血の時に赤血球が増産されたりするのもこのサイトカインの働きによる。血液のもとになる造血幹細胞や前駆細胞な細胞が特別な機能を持った赤血球や白血球などに変化する際には、このようなサイトカインの働きが必要であると考えられている。 - ※6 プロモーターやエンハンサー
いずれも遺伝子の働きを調節するためのDNA配列のこと。プロモーターは遺伝子の比較的近くにあって、ここにRNA合成酵素が結合し遺伝情報のコピーであるメッセンジャーRNAが合成される(これを転写という)。エンハンサーは遺伝子からやや離れた場所にあって、転写の効率を上げる作用を持つ。いずれの部分にも転写因子と呼ばれる転写効率を変化させるタンパク質が結合し、遺伝子からタンパク質が作られる量をコントロールしている。OCT4はこのような転写因子のひとつとして知られている。
Copyright © Keio University. All rights reserved.
