- ホーム
- 今月のサイエンス一覧
-
今月のサイエンス
今月のサイエンス - 2023年03月
1: Microenvironmental modulation in tandem with human stem cell transplantation enhances functional recovery after chronic complete spinal cord injury
Biomaterials.
2023 Jan 26;295:122002. doi: 10.1016
Shogo Hashimoto, Narihito Nagoshi, Munehisa Shinozaki, Katsuyuki Nakanishi, Yu Suematsu, Takahiro Shibata, Momotaro Kawai 4, Takahiro Kitagawa 4, Kentaro Ago, Yasuhiro Kamata, Kaori Yasutake, Ikuko Koya, Yoshinari Ando, Aki Minoda, Tomoko Shindo, Shinsuke Shibata, Morio Matsumoto, Masaya Nakamura, Hideyuki Okano

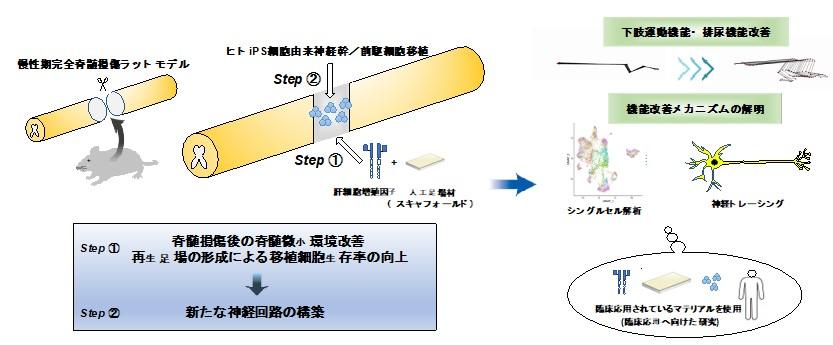
脊髄損傷患者の大多数を占める慢性期完全脊髄損傷に対しては、動物実験においてさえも有効な治療法がなく、私等は幹細胞移植と他の治療法との併用療法の開発を模索して来た。細胞移植単独療法は、様々な神経再生阻害因子により移植細胞の生着率が悪く、機能改善は乏しい。従って、移植細胞の効果を発揮させるために、移植前の脊髄微小環境を変化させることが重要な治療戦略である。
本研究では、慢性期完全損傷ラットモデルに対して肝細胞増殖因子含有徐放型スキャフォールド設置後、ヒトiPS由来神経幹前駆細胞移植を行い、下肢運動機能機能の回復を得ることに成功した。スキャフォールドを先に設置することで脊髄環境の改善と再生の足場を作り、その後細胞移植を行うことで移植細胞の生着率を向上させ、新たな神経回路の構築により、下肢運動機能の改善を認めた。本研究は、慢性期完全損傷に対する有効な治療法の一つとなり得る有意義な研究である。
(整形外科学教室 橋本将吾 93回、生理学教室 62回、整形外科学教室 名越慈人 81回)
2: Subarachnoid hemorrhage triggers neuroinflammation of the entire cerebral cortex, leading to neuronal cell death
Inflamm Regen.
2022 Dec 14;42(1):61. doi: 10.1186
Yamada H, Kase Y*, Okano Y, Kim D, Goto M, Takahashi S, Okano H**, Toda M**
* senior author ** corresponding author

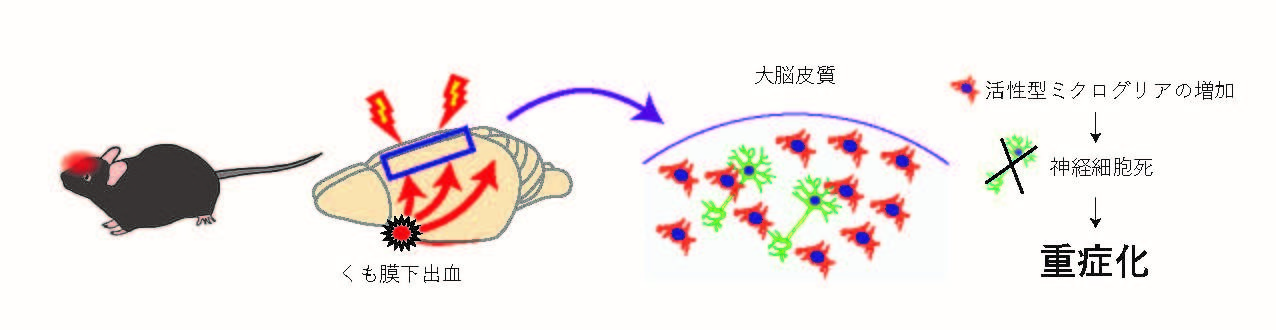
本論文では、くも膜下出血の発症早期に大脳皮質全体に神経炎症が及ぶことで神経細胞死が生じて、重症となることを明らかにした。くも膜下出血は、現代でも死亡率が高い疾患であり、発症早期の神経損傷に対する有効な治療法は確立していない。
筆者らは、重症度別のくも膜下出血のモデルマウスを作成し、作成24時間後に病巣近傍のみならず、遠位の大脳皮質においても神経炎症、並びに神経細胞死が生じていることを発見した。くも膜下出血の発症早期の障害が重要であることはこれまでに注目されていたが、神経炎症は出血が生じた近傍に限定されず、脳全体に波及して、神経細胞死が起きていることはわかっていなかった。
本結果は、くも膜下出血発症後の急性期での大脳皮質全体の炎症抑制が神経細胞の保護に効果的であることを示唆する結果である。研究グループはどのように神経炎症を抑えれば効果的な治療になり得るかの検討を始めている。
(脳神経外科学教室 山田浩貴 94回、戸田正博 66回、生理学教室 加瀬義高 91回相当、岡野栄之 52回)
3: IDH2 stabilizes HIF-1a-induced metabolic reprogramming and promotes chemoresistance in urothelial cancer
EMBO J.
2023 Feb 15;42(4):e110620. doi: 10.15252
Keisuke Shigeta, Masanori Hasegawa*, Takako Hishiki, Yoshiko Naito, Yuto Baba, ShujiMikami, Kazuhiro Matsumoto, Ryuichi Mizuno, AkiraMiyajima, Eiji Kikuchi, Hideyuki Saya, Takeo Kosaka** & Mototsugu Oya***

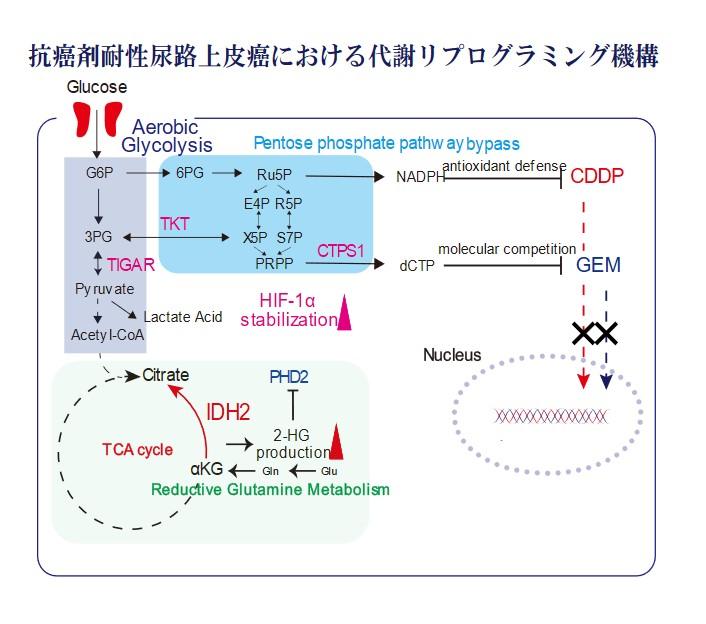
抗癌剤耐性後尿路上皮癌(Urothelial Carcinoma:UC)は泌尿器科癌の中で最も難治性な癌の1つであるが、本研究では化学療法(Gemcitabine / Cisplatin) 耐性獲得後の代謝ネットワーク制御機構を尿路上皮癌で初めて発見した報告である。本学設置のメタボロミクスコアを用いて網羅的メタボローム解析から、抗癌剤耐性株は、グルタミン代謝亢進に伴い逆行性にTCA回路を駆動させ、oncometaboliteである2-ヒドロキシグルタル酸(2-HG)が蓄積した結果Hif-1αの分解を抑制し、20%酸素下での嫌気解糖系代謝経路を活性化するという代謝リプログラミングを起こしており、この結果として抗癌剤への薬物的拮抗および活性酸素に対する抗酸化作用の増強をもたらすことを見いだした。この一連の代謝リプログラミング機構は、メタボリックチェックポイント分子として近年着目されてきているイソクエン酸デヒドロゲナーゼ2(IDH2)を軸として制御されており、IDH2の機能制御・阻害により抗癌剤の治療効果を大きく向上させることを見出した。本成果は、UC患者への化学療法治療感受性の向上へ波及効果が期待されます。
(泌尿器科学教室 小坂威雄 79相当)
その他の掲載論文
1: Loss of epigenetic information as a cause of mammalian aging
Cell.
2023 Jan 19;186(2):305-326.e27. doi: 10.1016
Jae-Hyun Yang, Motoshi Hayano, Patrick T Griffin, João A Amorim, Michael S Bonkowski, John K Apostolides, Elias L Salfati, Marco Blanchette, …Andreas R Pfenning, Luis A Rajman, David A Sinclair
2: Erratic and blood vessel-guided migration of astrocyte progenitors in the cerebral cortex.
2022 Nov 2;13(1):6571.
Tabata H, Sasaki M, Agetsuma M, Sano H, Hirota Y, Miyajima M, Hayashi K, Honda T, Nishikawa M
3: Changes in telepsychiatry regulations during the COVID-19 pandemic: 17 countries and regions' approaches to an evolving healthcare landscape.
2022;52(13):2606-2613.
Kinoshita S, Cortright K, Crawford A, Mizuno Y, Yoshida K, Hilty D, Guinart D, Torous J, Correll CU, Castle DJ, Rocha D, Yang Y, Xiang YT, Kolbaek P, Dines D, ElShami M, Jain P, Kallivayalil R, Solmi M, Favaro A, Veronese N, Seedat S, Shin S, de Pablo GS, Chang CH, Su KP, Karas H, Kane JM, Yellowlees P, Kishimoto T.
4: Early postoperative non-steroidal anti-inflammatory drugs and anastomotic leakage after oesophagectomy.
2023 Jan 10;110(2):260-266.
Hirano Y, Konishi T, Kaneko H, Itoh H, Matsuda S, Kawakubo H, Uda K, Matsui H, Fushimi K, Daiko H, Itano O, Yasunaga H, Kitagawa Y.
5: Mod(mdg4) variants repress telomeric retrotransposon HeT-A by blocking subtelomeric enhancers.
2022 Nov 11;50(20):11580-11599.
Takeuchi C, Yokoshi M, Kondo S, Shibuya A, Saito K, Fukaya T, Siomi H, Iwasaki YW.


