- ホーム
- 拠点リーダーからのご挨拶
- 幹細胞医学とは
- 幹細胞医学教育研究センター
- 5つの領域・サブグループ
- 事業推進担当者一覧
- 若手研究者情報
- COEX MEETING
- プレスリリース(抜粋)/発表論文情報
- KORD[研究者成果登録]
プログラム終了に当たって

池田康夫 (いけだやすお)

(2009年3月まで)慶應義塾大学大学院医学研究科 内科学 教授
(2009年4月から)早稲田大学先端生命医科学センター
Yasuo Ikeda, MD, PhD
yikeda@sc.itc.keio.ac.jp
http://www.keio-hematology.jp/
GCOE研究テーマ(役割分担)と研究計画
「造血幹細胞の未分化状態と血球分化の制御法開発および細胞医療への応用」
血液細胞の分化は、多分化能および自己複製能をもつ造血幹細胞(HSC)を頂点とし、多段階の運命決定を経て特定の血球系列(白血球・赤血球・血小板など)へ変化してゆく一連の過程である。HSCは骨髄中のニッチとよばれる微小環境に存在し、ニッチの様々なシグナルにより未分化状態に保たれている。血球産生の需要が高まるとHSCはニッチから動員され、分化・増殖し各種血球産生を行う。その後の血球分化にはC/EBPα, GATA-1などさまざまな転写因子が重要な役割を果たしており、これらにより各分化段階での運命決定がなされる。このような分化過程は従来不可逆的と考えられてきたが、我々の研究で分化形質は必ずしも絶対的なものではなく、可塑性を有することが明らかとなってきた。
本研究では、HSCの未分化性維持から成熟血球分化に至る一連の生理的プログラムを転写因子やニッチ因子を制御することで人為的に操作し、1)血球のリプログラミングによる多能性血球前駆細胞の創出、2)HSCの体外増幅、を行うことを目標にしている。これにより造血幹細胞移植や輸血医療に応用可能な臨床グレードの新たな細胞ソースを作り出すことを目指している。
略歴
昭和43年3月 |
慶応義塾大学医学部卒業 |
昭和48年7月 |
米国ブラウン大学医学部へ留学 |
昭和51年9月 |
慶應義塾大学医学部内科学教室に帰室 |
昭和57年7月 |
慶應義塾大学専任講師(医学部輸血センター) |
平成3年4月 |
慶應義塾大学教授(医学部内科学) |
平成7年10月 |
慶應義塾大学病院副院長(平成11年9月末日まで) |
平成11年10月 |
慶慶應義塾大学医学部長補佐(平成13年9月末日まで) |
平成13年10月 |
慶應義塾大学総合医科学研究センター長 現在に至る |
主たる研究領域
血栓止血学(特に血小板)、血液腫瘍学
主たる所属学会
日本内科学会 |
理事、2006年度学術集会会頭、在り方委員会委員長 |
日本血液学会 |
常任理事、倫理診療等委員会委員長、在り方委員会委員 |
日本動脈硬化学会 |
理事 |
日本脈学会 |
理事 |
日本造血細胞移植学会 |
理事、在り方委員会委員 |
日本血栓止血学会 |
理事、2003年度年次大会総会長 |
日本臨床血液学会 |
代表幹事、在り方委員会委員長、2002年第44回総会長 |
日本輸血学会 |
常任理事、倫理委員会委員、2001年度年次総会会長 |
A member, The International Society of Thrombosis and Haemostasis (ISTH)
The President, 23rd ISTH Congress 2011 (will be held in Japan)
ISTH'S Council Member (Class 2004 from 1998 till 2004)
A member, American Society of Hematology (ASH)
ASH's Corresponding Member's Council for 1998~1999
主たる公職
厚生労働省薬事・食品衛生審議会会員 平成13年12月27日より17年1月22日まで
薬事分科会員 平成14年9月30日より17年1月22日まで
医薬品第2部会部会 部会長、血液事業会員、医薬品等安全対策部会 部会会長代理、適正使用調査会委員長、生物由来製品臨時部会会員
医薬品副作用被害救済・研究振興調査機構 基礎研究委員会専門委員 平成15年6月~16年3月末日
血液製剤調査機構委員 平成3年より現在に至る
日本臍帯血バンクネットワーク事業運営委員会 平成11年10月より今に至る
賞罰
an Investigator Recognition Awards:
The "Ninth Biennial Awards for Contributions to Hemostasis"
at the 17th Congress of the International Society on Thrombosis and Hemostasis at Washington D.C., USA in August 1999
特記事項
日本医学会臨床幹事、日本内科学会監事、日本血液学会理事長、日本血栓止血学会理事長、
アジア太平洋血栓止血学会理事長、第23回国際血栓止血学会会長
研究協力者
山根 明子(COE RA)、古屋 善章(COE RA)、青木 亮子(COE RA)、花岡 洋成(COE RA)、髙田 哲也(COE RA)、鈴木 美佐子(COE RA)、淡谷 典弘(COE PD)、座間 猛(COE 特別研究講師)、宮川 義隆(内科学)、中村 隆典(内科学)、森 毅彦(内科学)、岡本 真一郎(内科学)、桑名 正隆(内科学)、伊藤 圭介(スローンケタリング記念研究所)、須田 年生(発生・分化生物学)、野村 達次(実験動物中央研究所)
これまでの研究成果
我々は血球転写因子による血球分化制御機構の解明に一貫して取り組んでおり、特にC/EBP, PU.1ファミリー転写因子による骨髄系分化誘導メカニズムを中心に研究を進めている。この中で、骨髄系転写因子であるC/EBPαをリンパ系・赤芽球系などの細胞で異所性に発現させるとこれらの細胞が骨髄系にリプログラミングされることを世界に先駆けて報告し、成熟血球が分化の可塑性を保持していることを明らかにした。また系列特異的と考えられてきたこれら転写因子が造血幹細胞でも機能しており、自己複製能を負に制御していることも報告している。
骨髄ニッチによる造血幹細胞制御機構の研究では、細胞外マトリックス制御因子であるTIMP-3が造血幹細胞の自己複製と静止状態維持を制御しており、骨髄抑制時における造血幹細胞の細胞周期動員と血球回復に重要な役割を果たしていることを明らかにした。

Fig.1 C/EBPαによる血球系列転換
C/EBPαの活性を異所性に誘導することにより、リンパ系・赤芽球系細胞を骨髄系に転換することができる。
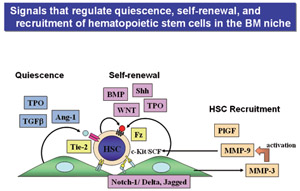
Fig.2 骨髄ニッチによる造血幹細胞の制御
ニッチから産生される様々なサイトカイン・増殖因子・細胞膜蛋白により造血幹細胞の静止状態・自己複製・細胞周期動員が制御されている。
COE内共同研究
- 脊免疫不全動物を用いたヒト造血幹細胞移植研究(実験動物中央研究所)
- 造血幹細胞の未分化性維持機構の解明(慶應義塾大学(坂口光洋記念講座)発生・分化生物学教室)
代表論文
- Yamane A, Nakamura T, Suzuki H, Ito M, Ohnishi Y, Ikeda Y, Miyakawa Y:Interferon-alpha2b-induced thrombocytopenia is caused by inhibition of platelet production but not proliferation and endomitosis in human megakaryocytes. Blood 112, 542-550, 2008.
- Mori T, Aisa Y, Watanabe R, Yamazaki R, Kato J, Shimizu T, Shigematsu N, Kubo A, Yajima T, Hibi T, Ikeda Y, Okamoto S: Long-term follow-up of allogeneic hematopoietic stem cell transplantation for de novo acute myelogenous leukemia with a conditioning regimen of total body irradiation and granulocyte colony-stimulating factor-combined high-dose cytarabine. Biol Blood Marrow Transplant 14: 651-657, 2008.
- Nogami W, Yoshida H, Koizumi K, Yamada H, Abe K, Arimura A, Yamane N, Takahashi K, Yamane A, Oda A, Tanaka Y, Takemoto H, Ohnishi Y, Ikeda Y, Miyakawa Y: A novel, small non-peptidyl molecule butyzamide activates human thrombopoietin receptor and promotes megakaryopoiesis. Haematologica 93, 1495-1504, 2008.
- Kimura N, Miyakawa Y, Kohmura K, Umezawa K, Ikeda Y, Kizaki M: Targeting NF-kB and induction of apoptosis by novel NF-kB inhibitor dehydroxymehylepoxyquinomycin (DHMEQ) in Burkitt lymphoma cells. Leuk Res. 31, 1529-1535, 2007.
- Mori T, Aisa Y, Yokoyama A, Nakazato T, Yamazaki R, Shimizu T, Mihara A, Kato J, Watanabe R, Takayama N, Ikeda Y, Okamoto S: Total body irradiation and granulocyte colony-stimulating factor-combined high-dose cytarabine as a conditioning regimen in allogeneic hematopoietic stem cell transplantation for advanced myelodysplastic syndrome: a single-institute experience. Bone Marrow Transplant 39: 217-221, 2007.
Copyright © Keio University. All rights reserved.
